
| A. | 一定浓度氢氧化钠溶液的配制(托盘天平、烧杯、温度计) | |
| B. | 蛋白质的盐析(试管、醋酸铅溶液、鸡蛋白溶液) | |
| C. | 钠的焰色反应(铂丝、氯化钠溶液、稀盐酸) | |
| D. | 乙酸的酯化反应实验(酒精灯、浓硫酸、浓盐酸) |
分析 A.根据各仪器的作用选取仪器;
B.醋酸铅溶液是重金属盐能使蛋白质发生变性;
C.根据钠的焰色反应所需仪器和操作步骤进行解答;
D.酯化反应需要用浓硫酸做催化剂.
解答 解:A.配制一定物质的量浓度的溶液时,用烧杯溶解药品,用托盘天平称量药品,用胶头滴管定容,所以不需要使用的仪器是温度计,故A错误;
B.向鸡蛋清中加入饱和硫酸铵溶液,可以观察到的现象为析出沉淀,说明饱和硫酸铵溶液可使蛋白质的溶解性变小,此过程叫做蛋白质的“盐析”为物理变化,蛋白质受热或遇到浓硝酸、重金属盐、甲醛等化学物质,会发生化学变化,失去原有的生理功能,此过程叫做蛋白质的“变性”,因此,醋酸铅重金属盐溶液能使蛋白质发生变性,故B错误;
C.做焰色反应实验前铂丝要用稀盐酸洗涤,再灼烧至跟酒精灯火焰颜色相同后再蘸取NaCl溶液,进行焰色反应,故C正确;
D.酯化反应需要用浓硫酸做催化剂,用不到浓盐酸,故D错误;
故选C.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:解答题
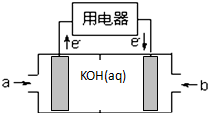 现有部分短周期元素的性质或原子结构如表:
现有部分短周期元素的性质或原子结构如表:| 元素编号 | 元素性质或原子结构 |
| A | 原子序数最小的元素 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | 最外层电子数比次外层电子数多3 |
| D | 单质的一种同素异形体是保护地球地表环境的重要屏障 |
| E | 最高正化合价为+7 |
| F | 第3周期元素原子半径 最大 |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题


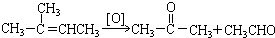
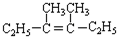 在上述类似条件下发生反应,请写出反应的方程式
在上述类似条件下发生反应,请写出反应的方程式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.153 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、 -3 | +7、 -1 | +5、 -3 | -2 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第3周期元素的简单离子中半径最小 |
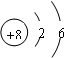 ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 次氯酸和臭氧都是强氧化剂,都能杀死水中的细菌.自来水常用氯气来杀菌消毒,是因为氯气杀菌消毒效果要比臭氧好,且不会残留有毒、有害物质 | |
| B. | 人们应用原电池原理,制成了多种电池,如干电池、充电电池、高能电池等.电池在现代生产和科学技术中发挥了重要作用,但废旧电池会对生态环境和公众健康造成危害,所以废旧电池必须回收再利用 | |
| C. | 明矾常用作净水剂,但人体摄入大量铝盐,易患老年性痴呆,所以明矾不宜大量作净水剂使用 | |
| D. | 氟氯烃为一类含有氟和氯的有机物,是制冷效果极佳的制冷剂,但它会破坏臭氧层,科研人员正在积极研发环保型的替代产品以减少氟氯烃的使用量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com