
����Ŀ����֪2Mg+CO2![]() 2MgO+C,ijͬѧ���ݽ����˳����Ʋ�����CO2Ҳ�ܷ�Ӧ��Ϊ̽����Ӧ���������ͼװ�ý���ʵ�顣(��֪PdCl2�ܱ�CO��ԭΪ��ɫ��Pd,����NaHCO3��Һ�������ڳ�ȥCO2 �е�HC1����)
2MgO+C,ijͬѧ���ݽ����˳����Ʋ�����CO2Ҳ�ܷ�Ӧ��Ϊ̽����Ӧ���������ͼװ�ý���ʵ�顣(��֪PdCl2�ܱ�CO��ԭΪ��ɫ��Pd,����NaHCO3��Һ�������ڳ�ȥCO2 �е�HC1����)
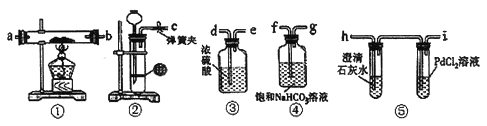
��1��ԭ���еĽ�����ͨ��������______�У�ʵ����ȡ��������������Ҫ�õ���ʵ����Ʒ��_____��____������Ƭ��С���ȡ�
��2��װ�â�����ϡ������CaCO3��Ӧ�Ʊ�CO2,�Ʊ�������ʱ������Ӧ�����ӷ���ʽ��___________��
��3���뽫ͼ�и�װ�ð�˳������(���b�ýӿ���ĸ): c��____��____��____��____��____��_____��______��
��4��װ�â۵�������___________��
��5�������װ�������Բ�װ��ҩƷ��ȼ�ƾ���֮ǰӦ���еIJ����Ǵ��ɼУ���CO2��������װ�ã����۲쵽________ʱ�ٵ�ȼ�ƾ��ơ��˲�������Ŀ����__________��
��6����������ʵ�������ƲⲢ��д������CO2��Ӧ�Ļ�ѧ����ʽ___________��
I.ʵ����������۲쵽װ�â�PdCl2��Һ���к�ɫ��������װ�â��й���ɷ�ֻ��һ�֣�������м���ϡ����ɲ�����ʹ����ʯ��ˮ���������塣��д������CO2��Ӧ�Ļ�ѧ����ʽ____________��
���𰸡� ú�� ��ֽ ���� CaCO3 + 2H+= Ca2++ H2O + CO2�� f g d e a b h ��ȥ������̼�л��е�ˮ���� ����װ�â��г���ʯ��ˮ��ʼ����� �ž�װ���еĿ��������������O2��H2O ����ʵ�� 2Na+2CO2![]() Na2CO3+ CO 4Na+3CO2
Na2CO3+ CO 4Na+3CO2![]() 2Na2CO3+ C
2Na2CO3+ C
����������1����Ϊ�ƿ��Ժ�ˮ��������Ӧ������ͨ��������ú���У�ȡ�ý�����ʱ������ȡС�飬������ֽ�����ɱ����ú�ͣ���С���гɶ�����С��С�飬����ʵ���� ��2��̼��ƺ����ᷴӦ�����Ȼ��ƺ�ˮ�Ͷ�����̼�����ӷ���ʽΪ�� CaCO3 + 2H+= Ca2++ H2O + CO2�� ��3������ȡ������̼�����к����Ȼ����ˮ������Ϊ�˷�ֹ�Ȼ����ˮ��������ʵ�飬Ӧ�����ȥ����������̼�����Ƴ�ȥ�Ȼ������壬����Ũ�����ȥˮ������������ʵ���ƺͶ�����̼�ķ�Ӧ����Ӧ���ܲ�����̼�������Ķ�����̼��Ӧ����һ����̼����������еij���ʯ��ˮ���ն�����̼�����Ȼ�Ǧ�����Ƿ����һ����̼���壬���������ӿ�����˳��Ϊ�� f �� g��d ��e �� a��b �� h����4��װ������Ϊ�˳�ȥ������̼�л��е�ˮ������5����Ϊװ���еĿ���Ҳ�����ʵ�飬Ӧ���ö�����̼�ų�������������̼���������Ʒ�Ӧ����̼��Ƴ��������Դ�Ϊ������װ�����г���ʯ��ˮ��ʼ��������ž�װ���еĿ��������������O2��H2O ����ʵ�飻��6��װ�â�PdCl2��Һ���к�ɫ������˵����Ӧ���ɵ�һ����̼����װ�â��й���ɷ�ֻ��һ�֣�������м���ϡ����ɲ�����ʹ����ʯ��ˮ���������壬˵������Ϊ̼���ƣ���Щ˵���ƺͶ�����̼��Ӧ���ܲ����IJ���Ϊ̼���ƺ�һ����̼��̼���ƺ�̼��̼�ٺͶ�����̼��Ӧ����һ����̼���ʷ���ʽΪΪ��2Na+2CO2![]() Na2CO3+ CO ��4Na+3CO2
Na2CO3+ CO ��4Na+3CO2![]() 2Na2CO3+ C��
2Na2CO3+ C��


 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. �ޡ�˿��ë����֬������Ȼ�л��߷��ӻ�����
B. ������ϩ���Ͽ��������߲�ˮ������ʳ�ȵı���Ĥ
C. ��ά�ء����۶�����(C6H10O5)n��ʾ�����ǻ�Ϊͬ���칹��
D. ���������£�������������������ͭ��Һ��ϼ��ȣ�����ש��ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������к��зḻ�Ŀ�̽�˾۱�ȼ��3He���º����������̲��ŷḻ���ѡ��������������ơ�þ��ͭ�Ƚ��������Դ�ʹ����Ķ������衢����ȣ���Ϊ�������Ŀɳ�����չ�������ס������й�������ȷ����(����)
A. �����ϵĶ�����������Ԫ�ض��ǵ�������Ԫ��
B. 3He�ɷ����˾۱䷴Ӧ������һ�ֻ�ѧ�仯
C. �����ϵ�3He��һ����Ԫ��
D. �ѡ�����ͭԪ�ض����ڹ���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������CO2����ͨ��ˮ����(Na2SiO3��Һ)�У�Ȼ��������ɣ����ڸ����³�����գ����õ��Ĺ���������(����)
A.Na2SiO3B.Na2CO3��Na2SiO3
C.Na2CO3��SiO2D.SiO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������������ά�ء�������ά�ص����ܼ���ʵ���Һϳɼ�����������ķ�Ӧԭ�����й��������£� ![]() +2C2H5OH
+2C2H5OH ![]()
![]() +2H2O
+2H2O
��Է������� | �ܶ�/��gcm��3�� | �е�/�� | ˮ���ܽ��� | |
����������� | 202 | 1.01 | 245 | ������ˮ |
������ | 146 | 1.36 | 231.8 | �� |
�Ҵ� | 46 | 0.79 | 78.4 | ���� |
�ױ� | 92 | 0.87 | 110.6 | ������ˮ |
ʵ�鲽�����£�
����1����50mLԲ����ƿ�м��뼺����1.8g��0.012mol�����Ҵ�4.4mL��0.076mol�����ױ�5mL��Ũ���ᣨ1mL����װ����ͼ��ʾ��С����Ȼ���40min��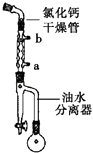
����2����ȴ������װ�ø�Ϊ����װ�ã���ѹ������120�����ҳ������
����3��������2��Һ�嵹�������ƿ�����м�ѹ�������ü����������2.2g��
��1��ͼ������������ȴˮ�����a����b�����ڽ���Ũ�������Ҫ������������ ��
��2������һ��ʱ���ͼ��������������������Ҫ�� ��
��3��ʵ���м���������Ҵ���Ŀ���� ��
��4������2ʵ������ɵı�־�� ��
��5����ʵ��IJ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������е��������ͺ�����������ֱ���ͬ����ô����������������( )
A.���ֲ�ͬ����B.һ�ַ��Ӻ�һ������
C.���ֲ�ͬ������D.���ֲ�ͬ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Է�������Ϊ128���л���A��ȫȼ��ֻ����CO2��H2O����A��һ����̼���ҿ���NaHCO3��Һ��Ӧ������һ�ȴ������ĿΪ�� ��
A.2
B.3
C.4
D.5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��D��E��G��������ɵĸ���W�Ļ�ѧʽΪxAaDdyE2DzG��4.704g W����ˮ��һ�������������Һ��������������Ϊ3.408g��ͬ������W��5.13g����������ֻ��Ⱥ���ȣ����ɵ�����������������Һ������յ�Al��OH��3 0.624g�����Ⱥ�IJ�����ˮ����ܽ����ˣ���Һ�Է�̪Ϊָʾ����0.400mol/L H2SO4�ζ����յ㣬��ȥH2SO4 15.0mL���ζ���Ϻ���Һ�м�ⲻ���κν������Ӻ�������ӣ�����������ϴ��ʱ�����ܽ⣬��һ��ʯ̿������ɫ�Ļ�ɫ��Һ�����������ͼ����жϣ�
��1�������D��E��G����������������
��2��a��d�ı�ֵΪ��
��3�����εĻ�ѧʽΪ �� ��д�����㲽�裩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Լ����Ⱥ�˳��,�ɽ����ᡢH2SO4��K2SO4��NaOH��KNO3������ɫ����Һ����������
A. ��ɫʯ����Һ��AgNO3��Һ��ϡ���� B. BaCl2��Һ����ɫ��̪��Һ��AgNO3��Һ
C. ��ɫʯ����Һ��BaCl2��Һ D. ��ɫ��̪��Һ��BaCl2��Һ��AgNO3��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com