
工业上常利用反应 3Cl2+8NH3 =6NH4Cl+N2 检查氯气管道是否漏气。回答下列问题:
(1)该反应中,氧化剂是 ,发生氧化反应的物质是 。
(2)该反应中氧化剂与还原剂的物质的量之比为 。
(3)若标准状况下有6.72L N2生成,则转移电子的物质的量为 mol。
(1)Cl2 NH3 (写物质名称也可) (2)3:2 (3)1.8
解析试题分析:(1)根据反应的方程式可知,氯元素的化合价从0价降低到-1价,得到1个电子,氯气是氧化剂;氨气中氮元素的化合价从-3价升高到0价,失去3个电子,氨气是还原剂,发生氧化反应。
(2)根据电子的得失守恒可知,该反应中氧化剂与还原剂的物质的量之比为3:2。
(3)标准状况下6.72L N2的物质的量是6.72L÷22.4L/mol=0.3mol,所以转移电子的物质的量为0.3mol×6=1.8mol。
考点:考查氧化还原反应的有关计算与判断
点评:该题是中等难度的试题,也是高考中的常见题型和重要的考点之一,侧重对基础知识的巩固与训练的,难度不大。该题的关键是准确判断出有关元素的化合价变化情况,然后根据有关概念灵活运用、分析、判断即可。


科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
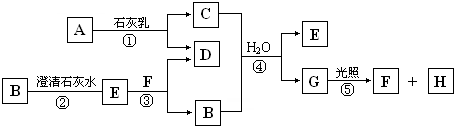
 (2013?中山一模)现有A~G七种物质,已知A是赤铁矿的主要成分,E的浓溶液稀释时会放出大量的热,G溶液为蓝色,它们之间存在如右图所示的转化关系:
(2013?中山一模)现有A~G七种物质,已知A是赤铁矿的主要成分,E的浓溶液稀释时会放出大量的热,G溶液为蓝色,它们之间存在如右图所示的转化关系:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

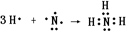
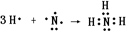
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
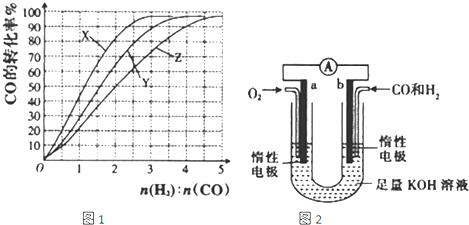
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com