
【题目】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装 置的开关时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为_____(填“原电池”“电解池”或“电镀池”),通入 CH3OH 电极的电极反应为_____。
(2)乙池中 A(石墨)电极的名称为_____(填“正极”“负极”或“阴极”“阳极”),总反应为__________。
(3)当乙池中 B 极质量增加 5.4 g 时,甲池中理论上消耗 O2 的体积为_____mL(标准状 况),丙池中_____(填“C”或“D”)极析出_____g 铜。
(4)若丙中电极不变,将其溶液换成 NaCl 溶液,开关闭合一段时间后,甲中溶液的 pH将_____(填“增大”“减小”或“不变”,下同),丙中溶液的 pH 将______。
【答案】(1)原电池 O2+4e+2H2O=4OH
(2)阴极 2CuSO4+2H2O![]() 2H2SO4+2Cu+O2↑ (3)280 F 1.6 (4)减小 增大
2H2SO4+2Cu+O2↑ (3)280 F 1.6 (4)减小 增大
【解析】
(1)甲池为燃料电池,是原电池,A为负极,B为正极,发生还原反应,B电极的电极反应式为O2+4e+2H2O=4OH;
(2)丙池为电解池,其中F电极为阴极,电解硫酸铜溶液的方程式为:2CuSO4+2H2O![]() 2H2SO4+2Cu+O2↑;
2H2SO4+2Cu+O2↑;
(3)根据转移电子数目相等,4Ag ~ O2,
4×108 g 22400 mL
5.4 g V
所以V=![]() mL ="280" mL;丙池中阴极F极析出Cu,根据电子守恒可知析出Cu的质量为
mL ="280" mL;丙池中阴极F极析出Cu,根据电子守恒可知析出Cu的质量为![]() ="1.6" g。
="1.6" g。
(4)甲中发生的反应为甲醇与氧气、氢氧化钾的反应,反应消耗氢氧根离子,则pH减小,丙中电极不变,将其溶液换成NaCl溶液,则丙中电解NaCl溶液生成氢氧化钠,所以溶液的pH增大。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ钠是一种活泼金属,能与很多物质反应,
(1)写出金属钠与水反应的化学方程式,并用双线桥标出电子转移的方向和数目__________________________________
(2)该反应的还原剂是_______,(填化学式,下同)
(3)该反应中被还原的元素是___________. (填元素符号),氧化产物是__________.
(4)若反应转移了0.4 mol电子,则产生的气体在标准状况下体积为____________L.
Ⅱ某研究小组同学为了探究硝酸的性质,进行了如下操作:
(1)从试剂柜里取一瓶浓硝酸,发现其保存在________色的试剂瓶里,原因是(用化学方程式表示)_________________________。打开瓶盖,小心地扇闻浓硝酸的气味。
(2)该研究小组欲用该浓硝酸(15 mol/L)来配制480mL 3 mol/L的稀硝酸,则需要量取的浓硝酸的体积是_________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某粉末状样品由铁、铝、铜三种金属组成,加入过量稀硫酸充分反应,过滤后向滤液中加入过量烧碱溶液,再过滤,滤液中存在的离子有( )
A. AlO2﹣ B. Fe2+ C. Fe3+ D. Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3.42g蔗糖与3.24g淀粉混合并完全水解,若共生成mg葡萄糖和ng果糖,则m:n为
A. 1:3 B. 1:5 C. 5:1 D. 3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
(1)钢铁腐蚀主要是吸氧腐蚀,试写出该腐蚀过程中的电极反应式:负极________;正极________。
(2)为了减缓某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用________(填序号)。
A.铜 B.钠
C.锌 D.石墨
(3)图乙所示的方案也可以减缓铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的________极。

图甲 图乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2017·天津卷)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过以下反应可获得新型能源二甲醚(![]() )。下列说法不正确的是
)。下列说法不正确的是
①![]()
![]()
②![]()
![]()
③![]()
![]()
④![]()
![]()
A. 反应①、②为反应③提供原料气
B. 反应③也是![]() 资源化利用的方法之一
资源化利用的方法之一
C. 反应![]() 的
的![]()
D. 反应![]() 的
的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁是一种重要的化工原料,可以制备一系列物质。下列说法错误的是( )
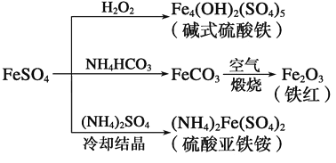
A. 碱式硫酸铁水解能产生 Fe(OH)3胶体,可用作净水剂
B. 为防止NH4HCO3 分解,生产FeCO3需在较低温度下进行
C. 常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4 的大
D. 可用KSCN溶液检验(NH4)2Fe(SO4)2 是否被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com