
| A.Fe3O4既可看做是氧化物,又可看做是亚铁盐 |
| B.反应②配平后,H2O的化学计量数为3 |
| C.反应③是非氧化还原反应 |
| D.碱性条件下,NaNO2的氧化性比Na2FeO2、Na2Fe2O4都强 |
科目:高中化学 来源:不详 题型:填空题
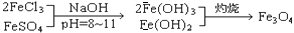
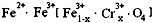 ,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为 。
,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
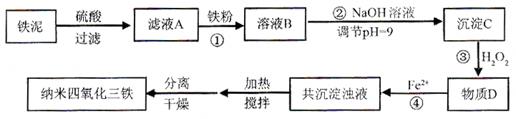
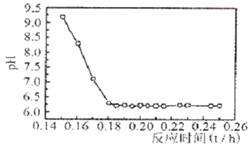
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 4Fe(OH)3+8OH-+3O2。
4Fe(OH)3+8OH-+3O2。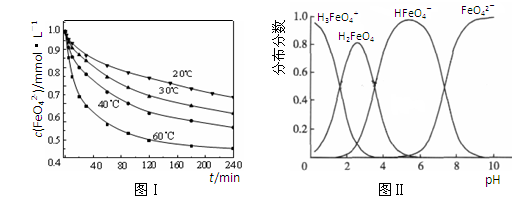

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2.8g | B.5.6g | C.11.2g | D.1.4g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com