
| A. | H2O2 | B. | Al(OH)3 | C. | FeCl2 | D. | H2SiO3 |
科目:高中化学 来源: 题型:选择题
| A. | 分液中,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 称量氢氧化钠固体时,将氢氧化钠固体放在垫有滤纸的托盘 | |
| C. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| D. | 称量时,砝码应放在托盘天平的右盘 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
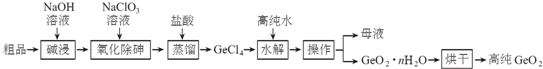
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气与水反应:Cl2+H2O═Cl-+ClO-+2H+ | |
| B. | 铁与盐酸反应:2Fe+6H+═3H2↑+2Fe3+ | |
| C. | 硫酸与氢氧化钡混合:2H++SO42-+Ba2++2OH?═Ba SO4↓+2 H2O | |
| D. | 向AlCl3溶液中滴入过量NaOH溶液:Al3++3OH-=Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O═2SO32-+4Cl-+6H+ | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═Fe3++2Fe2++4H2O | |
| C. | 加热可增强纯碱溶液去污力:CO32-+2H2O?H2CO3+2OH- | |
| D. | 过量CO2通入Ca(ClO)2溶液中:ClO-+CO2+H2O=HCO3-+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定浓度的氨水加水稀释的过程中,c(NH4+)/c(NH3•H2O)的比值减小 | |
| B. | 浓度均为0.1 mol•L-1的Na2CO3、NaHCO3混合溶液中:c(CO32-)<c(HCO3-),且3c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] | |
| C. | 0.2 mol•L-1的醋酸(CH3COOH)溶液与0.1 mol•L-1NaOH溶液等体积混合后:c(CH3COO-)+2 c(OH-)=c(CH3COOH)+2c(H+) | |
| D. | 常温下,已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2CrO4悬浊液中的c(Ag+)一定小于AgCl悬浊液中的c(Ag+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
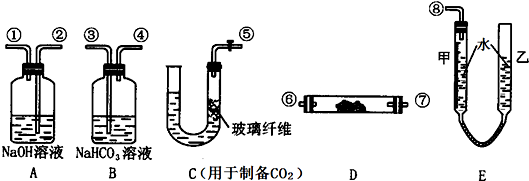
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com