
某主族元素的原子最外层电子排布是5S1,下列描述中正确的是
A.其单质常温下跟水反应不如钠剧烈 B.其原子半径比钾原子半径小
C.其碳酸盐易溶于水 D.其氢氧化物不能使氢氧化铝溶解
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
检验铵盐的方法是将待检物取出少量放入试管中,然后( )
A.加热,用湿润的红色石蕊试纸放在试管口检验
B.加水溶解,用红色石蕊试纸检验溶液的酸碱性
C.加入碱溶液,加热,再滴入酚酞试液
D.加入氢氧化钠溶液,加热,用湿润的红色石蕊试纸放在试管口检验
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要0.2 mol/L CuSO4溶液240 mL,实验室可提供配制溶液的试剂有:①蓝色胆矾晶体(CuSO4·5H2O) ②4mol/L CuSO4溶液
(1)、无论采用何种试剂进行配制,实验必须用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,至少还需要的一种仪器是________.
(2)、若用胆矾晶体进行配制,需用托盘天平称取CuSO4· 5H2O的质量为________g;如果用4mol/L的CuSO4溶液稀释配制,需用量筒量取___________ml 4 mol/L CuSO4溶液。
(3)、实验室用4mol/L的硫酸铜溶液稀释配制溶液所需的实验步骤有:
其中正确的操作顺序为
①往烧杯中加入约100ml水进行初步稀释,冷却至室温
②用量筒量取一定体积4mol/L 的硫酸铜溶液于一烧杯中
③计算所需4mol/L 硫酸铜溶液的体积
④将溶液颠倒摇匀后转存于试剂瓶
⑤加水至液面离容量瓶1-2cm处改用胶头滴管进行定容
⑥洗涤烧杯和玻璃棒2-3次并将洗涤液注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀
⑦将溶液转移入容量瓶
(4)、配制溶液过程中,如果出现以下情况,对结果有何影响(填“偏高”、“偏低”或“无影响”)
A.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
B.定容时俯视刻度线 _____________
C.容量瓶未干燥即用来配制溶液
D.量筒用蒸馏水洗后未干燥就用来量取4mol/L的CuSO4溶液________________
E.将烧杯中的溶液转移到容量瓶时,未用水洗涤烧杯 _______________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是
A.共价化合物中不可能含有离子键 B.有共价键的化合物,不一定是共价化合物
C.离子化合物中可能存在共价键 D.原子以极性键结合的分子,肯定是极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3.H2O.CH4三分子中键角大小顺序正确的是
A.NH3>H2O>CH4 B.CH4>NH3>H2O C.CH4>H2O>NH3 D.H2O>CH4>NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
A.B.C.D.E.F六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A可形成分子X,X的水溶液呈碱性;D的简单阳离子与X具有相同电子数,且D是同周期中简单离子半径最小的元素;基态E原子p能级上有一对成对电子,C.F两种元素的原子最外层共有13个电子。回答下列问题:
(1)D.E.F中电负性最大的是 (填写元素符号)。
(2)写出D原子的外围电子排图为 。
(3)B.C.E分别与A形成的化合物中沸点最高的是 。
(4)C与D形成的化合物的化学式是 ,请写出其溶于NaOH的离子方程式 ;
(5)F的单质在反应中常作 剂,该单质的水溶液与E的低价氧化物反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,SO2表现氧化性的是( )
A.2SO2+O2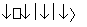 2SO3 B.SO2+H2OH2SO3
2SO3 B.SO2+H2OH2SO3
C.2H2S+SO2===3S↓+2H2O D.SO2+2H2O+Cl2===H2SO4+2HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
填空
(1)1 mol O原子中含有______________个O原子。
(2)3 mol H2SO4中含有__________个H2SO4,含有____________个H原子。
(3)4 mol O2含有__________ mol O原子,64 mol e-。
(4)6.02×1024个Na+的物质的量是________ mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com