
关于下列四个图像的说法中不正确的是

A.图①表示可逆反应:CO(g) + H2O(g) CO2(g)+ H2(g)ΔH <0
CO2(g)+ H2(g)ΔH <0
B.图②表示电解氯化钠的稀溶液,阴、阳两极产生气体体积之比可能是1∶1
C.图③表示可逆反应:A2(g)+ 3B2(g) 2AB3(g) ΔH <0
2AB3(g) ΔH <0
D.图④表示压强对可逆反应2A(g)+ 2B(g) 3C(g)+ D(s)的影响,乙的压强大
3C(g)+ D(s)的影响,乙的压强大
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
298K、10lkPa时,1molH2(g)与O2(g)完全反应生成H2O(g)时放出242kJ热量,而生成H2O(1)时放出286kJ热量,则下列表达不正确的是( )
|
| A. | 2H2(g)+O2(g)=2H2O(g);△H=﹣484kJ•mol﹣1 | B. | H2O(g)=H2(g)+O2(g);△H=242kJ•mol﹣1 |
|
| C. | H2(g)+O2(g)=H2O(1);△H=﹣286kJ•mol﹣1 | D. | H2O(1)=H2O(g);△H=﹣44kJ•mol﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A(g)+2B(g)=C(g)的反应过程中能量变化如右下图所示。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。下列相关说法正确的是

A.该反应是吸热反应
B.催化剂改变了该反应的焓变
C.催化剂降低了该反应的活化能
D.该反应的焓变△H=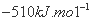
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:A、B、C、D、E为周期表1~36号中的元素,它们的原子序数逐渐增大。A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;C2—离子D2+离子具有相同的、稳定的电子层结构;E的基态原子的外围电子排布式为3d84s2。
请回答下列问题:
⑴A、B、C、D四种元素中,电负性最大的是 (填元素符号)。
⑵B的氢化物的沸点远高于A的氢化物的主要原因是 。
⑶由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-中A原子的杂化方式为 。
 ⑷E2+离子能与AC分子形成[E(AC)4]2+,其原因是AC分子中含有 。
⑷E2+离子能与AC分子形成[E(AC)4]2+,其原因是AC分子中含有 。
⑸最近发现,只含A、D、E三种元素的一种晶体(晶胞如右图所示)具有超导性。A原子的配位数为 ;该晶体的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,可逆反应X(g)+3Y(g)  2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol /L,0.3mol/ L,0.08 mol/L,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol /L,0.3mol/ L,0.08 mol/L,则下列判断不合理的是
A.c1:c2=1:3 B.平衡时,Y和Z的生成速率之比为3:2
C.X、Y的转化率不相等 D.c1的取值范围为0< c1 <0.14 mo /L
查看答案和解析>>
科目:高中化学 来源: 题型:
最新研制的一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池。下列有关此
电池的叙述错误的是
A.正极电极反应:
B.负极电极反应: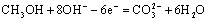
C.电池在使用过程中电解质溶液的pH降低
D.当外电路通过0.6 电子时,理论上消耗甲醇6.4g
电子时,理论上消耗甲醇6.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
现代工业将煤炭气化,既可以提高燃料的利用率、减少CO、SO2等的排放,又可以扩大水煤气的广泛用途。
⑴已知:2C(s)+O2(g)=2CO(g);ΔH1 , 2H2(g)+O2(g)=2H2O(g);ΔH2 。
则反应C(s)+H2O(g)  CO(g)+H2(g);ΔH= 。(用含ΔH1、ΔH2
CO(g)+H2(g);ΔH= 。(用含ΔH1、ΔH2
的代数式表示)
(2)制甲醇所需要的氢气,可用下列反应制取:
H2O(g)+CO(g) H2(g)+CO2(g)△H < 0 某温度下,该反应的平衡常数K=1。
H2(g)+CO2(g)△H < 0 某温度下,该反应的平衡常数K=1。
①该温度下,若起始时c(CO)= 1 mol/L, c(H2O)= 2 mol/L,反应进行一段时间后,测得H2的浓度为0.5 mol/L,则此时该反应v(正) v(逆) (填>、=、<)。
②若降低温度,该反应的K值将 。(填"增大"、"减小"或"不变" )
③据研究CO(g)+2H2(g) CH3OH(g),制备甲醇的反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: _______________________________________ (用化学方程式表示)。
CH3OH(g),制备甲醇的反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: _______________________________________ (用化学方程式表示)。
(3)CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)  CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。
CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。

①该反应的ΔH3 0(选填“<”、“>”或“=”,下同),K1 K2。
②将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有 。
(4)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态K2CO3为电解质。写出该燃料电池负极的电极反应式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
铜的摩尔质量为M g/mol,密度为ρ g/cm3,阿伏加德罗常数为NA,下列说法正确的是( )
A.1 kg铜所含原子的数目为ρ NA B.一个铜原子所占有的体积为M /(ρNA )cm3
C.一个铜原子的质量为 ρ M / NA g D.1 dm3铜所含有的原子数为 ρ NA / M
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中Cl-、Br-、I-三者物质的量之比是1:2:3,通入一定量的Cl2,当反应完全后,该比值变为3:2:1,则反应的Cl2和原溶液中I-的物质的量之比是( )
A. 1:2 B. 1:3 C. 1:4 D. 1:6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com