
| Ń”Ļī | ÄæµÄ | ³żŌÓŹŌ¼Į | ŹµŃé·½·Ø |
| A | ³żČ„CuCO3¹ĢĢåÖŠµÄ£ØNH4£©2CO3 | - | ÖĆÓŚŪįŪöÖŠ¼ÓČČÖĮŗćÖŲ |
| B | ³żČ„Ag2SÖŠÉŁĮæAgCl | Na2SČÜŅŗ | ¹żĀĖ |
| C | ³żČ„ŅŅĻ”ÖŠµÄSO2ĘųĢå | ĖįŠŌøßĆĢĖį¼ŲČÜŅŗ | Ļ“Ęų |
| D | ³żČ„øŹÓĶÖŠµÄŅŅĖį | NaOHČÜŅŗ | ·ÖŅŗ |
| A£® | A | B£® | B | C£® | C | D£® | D |
·ÖĪö A£®¼ÓČČŹ±Ģ¼ĖįĶŅ²·Ö½ā£»
B£®¼ÓČėĮņ»ÆÄĘČÜŅŗ£¬æÉÉś³ÉĮņ»ÆŅų³Įµķ£»
C£®¶žÕ߶¼æɱ»øßĆĢĖį¼ŲŃõ»Æ£»
D£®øŹÓĶ”¢ŅŅĖįČÜÓŚĖ®”¢ĒŅŅŅĖįÓėĒāŃõ»ÆÄĘ·“Ó¦£®
½ā“š ½ā£ŗA£®¼ÓČČŹ±Ģ¼ĖįĶŅ²·Ö½ā£¬¼ÓČČŹ±ĪĀ¶Č²»Äܹżøߣ¬¹ŹA“ķĪó£»
B£®¼ÓČėĮņ»ÆÄĘČÜŅŗ£¬ŅņĮņ»ÆŅų±ČĀČ»ÆŅųµÄČܶȻżŠ”£¬æÉÉś³ÉĮņ»ÆŅų³Įµķ£¬¹ŹBÕżČ·£»
C£®¶žÕ߶¼æɱ»øßĆĢĖį¼ŲŃõ»Æ£¬æÉÓĆĒāŃõ»ÆÄĘČÜŅŗ³żŌÓ£¬¹ŹC“ķĪó£»
D£®øŹÓĶ”¢ŅŅĖįČÜÓŚĖ®”¢ĒŅŅŅĖįÓėĒāŃõ»ÆÄĘ·“Ó¦£¬·“Ó¦ŗóČÜŅŗ²»·Ö²ć£¬²»ÄÜÓĆ·ÖŅŗµÄ·½·Ø·ÖĄė£¬¹ŹD“ķĪó£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²é»ģŗĻĪļ·ÖĄė”¢Ģį“æ·½·ØµÄŃ”ŌńŗĶÓ¦ÓĆ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĪļÖŹµÄŠŌÖŹ¼°·ÖĄė”¢Ģį“æ·½·ØĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ³żŌÓµÄ漲飬עŅā³żŌÓµÄŌŌņ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ūĻ©µÄ¼üĻߏ½£ŗ | B£® | CH2F2µÄµē×ÓŹ½£ŗ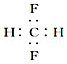 | ||
| C£® | Č©»ł¹ŁÄÜĶÅ·ūŗÅ£ŗ-COH | D£® | -OHÓė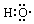 ¶¼±ķŹ¾ōĒ»ł ¶¼±ķŹ¾ōĒ»ł |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©µÄ½į¹¹¼ņŹ½ĪŖCH2CH2 | |
| B£® | ŌŚĖįŠŌĢõ¼žĻĀ£¬CH3CO18OC2H5µÄĖ®½ā²śĪļŹĒCH3CO18OHŗĶC2H5OH | |
| C£® | ±½ŗĶÅØĻõĖįµÄ·“Ó¦ÓėŅŅĻ©ŗĶBr2µÄ·“Ó¦ŹōÓŚĶ¬Ņ»ĄąŠĶµÄ·“Ó¦ | |
| D£® | æÉŅŌÓĆŠĀÖʵÄĒāŃõ»ÆĶŠü×ĒŅŗ¼ģŃéÄņŅŗÖŠŹĒ·ńŗ¬ÓŠĘĻĢŃĢĒ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ”÷H1£¾”÷H2 | |
| B£® | Éč¼Ę·“Ó¦¢ŁµÄÖ÷ŅŖÄæµÄŹĒŌö“ón£ØCO£©/n£ØH2£©µÄ±ČÖµ | |
| C£® | CO£Øg£©+H2O£Øg£©?CO2£Øg£©+H2£Øg£©µÄÕż·“Ó¦ĪŖĪüČČ·“Ó¦ | |
| D£® | ”÷H2=4”÷H1=659.3 KJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1mol Cl2²Ī¼Ó·“Ó¦×ŖŅʵē×ÓŹżŅ»¶ØĪŖ2NA | |
| B£® | 1mol NaHCO3¾§ĢåÖŠŃōĄė×ÓŹżĪŖ2NA | |
| C£® | ³£ĪĀ³£Ń¹Ģõ¼žĻĀ£¬14gŅŅĻ©ŗĶ¶”Ļ©»ģŗĻĪļŗ¬ÓŠµÄ¹²ÓƵē×Ó¶ŌŹżĪŖ3NA | |
| D£® | 1ml•L-1 NaClČÜŅŗÖŠŗ¬ÓŠµÄNa+ŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
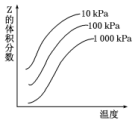 ČēĶ¼ŹĒĪĀ¶ČŗĶŃ¹Ēæ¶Ō·“Ó¦X+Y?2ZÓ°ĻģµÄŹ¾ŅāĶ¼£®Ķ¼ÖŠ×Ż×ų±ź±ķŹ¾Ę½ŗā»ģŗĻĘųĢåÖŠZµÄĢå»ż·ÖŹż£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø””””£©
ČēĶ¼ŹĒĪĀ¶ČŗĶŃ¹Ēæ¶Ō·“Ó¦X+Y?2ZÓ°ĻģµÄŹ¾ŅāĶ¼£®Ķ¼ÖŠ×Ż×ų±ź±ķŹ¾Ę½ŗā»ģŗĻĘųĢåÖŠZµÄĢå»ż·ÖŹż£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø””””£©| A£® | ŗćČŻŹ±£¬»ģŗĻĘųĢåµÄĆܶČæÉ×÷ĪŖ“Ė·“Ó¦ŹĒ·ń“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄÅŠ¶ĻŅĄ¾Ż | |
| B£® | X”¢Y”¢Z¾łĪŖĘųĢ¬ | |
| C£® | ÉĻŹö·“Ó¦µÄÄę·“Ó¦µÄ”÷H£¾0 | |
| D£® | Ź¹ÓĆ“ß»Æ¼ĮZµÄ²śĀŹĢįøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | µŚŅ»µēĄėÄÜ£ŗ¢Ū£¾¢Ś£¾¢Ł | B£® | Ō×Ó°ė¾¶£ŗ¢Ū£¾¢Ś£¾¢Ł | ||
| C£® | µēøŗŠŌ£ŗ¢Ū£¾¢Ł£¾¢Ś | D£® | ×īøß»ÆŗĻ¼Ū£ŗ¢Ś£¾¢Ł£¾¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬ĀČĘųµÄĦ¶ūÖŹĮæµČÓŚ71g | |
| B£® | 1molH2SO4ÖŠŗ¬ÓŠ2molĒāŌŖĖŲ | |
| C£® | ijĪļÖŹµÄĦ¶ūÖŹĮæ¾ĶŹĒøĆĪļÖŹµÄĻą¶Ō·Ö×ÓÖŹĮæ»ņĻą¶ŌŌ×ÓÖŹĮæ | |
| D£® | 2gŗ¤ĘųĖłŗ¬µÄŌ×ÓŹżÄæŌ¼ĪŖ0.5”Į6.02”Į1023 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŹµŃ鱹ŗÅ | ĪĀ¶Č/”ę | ĘšŹ¼Ź±ĪļÖŹµÄĮæ/mol | Ę½ŗāŹ±ĪļÖŹµÄĮæ/mol | |
| n£ØX£© | n£ØY£© | n£ØM£© | ||
| ¢Ł | 700 | 0.10 | 0.10 | 0.09 |
| ¢Ś | 800 | 0.20 | 0.20 | 0.10 |
| ¢Ū | 800 | 0.20 | 0.30 | a |
| ¢Ü | 900 | 0.10 | 0.15 | b |
| A£® | ŹµŃé¢ŁÖŠ£¬Čō5minŹ±²āµĆn£ØM£©=0.05mol£¬Ōņ0ÖĮ5minŹ±¼äÄŚ£¬ÓĆN±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØN£©=0.01 mol/£Ø L•min£© | |
| B£® | ŹµŃé¢ŚÖŠ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżK=1.0 | |
| C£® | ŹµŃé¢ŪÖŠ£¬“ļµ½Ę½ŗāŹ±£¬XµÄ×Ŗ»ÆĀŹĪŖ60% | |
| D£® | ŹµŃé¢ÜÖŠ£¬“ļµ½Ę½ŗāŹ±£¬b£¾0.06 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com