
分析 (1)根据两性氧化物能与酸反应生成盐和水;根据Be(NO3)2溶液中逐滴加入等浓度的NaOH先后发生反应:Be(NO3)2+2NaOH=Be(OH)2↓+2NaNO3,Be(OH)2+2NaOH═Na2BeO2+2H2O,先产生沉淀,然后沉淀消失,两次消耗的氢氧化钠的物质的量都为0.02mol(即20mLNaOH溶液),产生的Be(OH)2沉淀为0.01mol;
(2)①根据质量守恒书写方程式;
②A.GeO2与SiO2性质不相似,GeO2与盐酸反应,SiO2与盐酸不反应;
B.过程Ⅱ的蒸馏是利用GeCl4的沸点低来实现的;
C.过程Ⅳ发生的反应中,GeO2中Ge的化合价降低,作氧化剂;
D.过程Ⅰ、Ⅲ是复分解反应,过程Ⅳ是置换反应;
(3)将硫与浓硝酸混合,结果生成一种纯净无色气体A,A遇空气变红棕色,说明A为一氧化氮,由于浓硝酸的强氧化性,能将硫氧化成+6价的硫酸,然后根据质量守恒配平;
解答 解:(1)BeO与盐酸反应的生成氯化铍和水,反应的离子方程式为:BeO+2H+=Be2++H2O;Be(NO3)2溶液中逐滴加入等浓度的NaOH先后发生反应:Be(NO3)2+2NaOH=Be(OH)2↓+2NaNO3,Be(OH)2+2NaOH═Na2BeO2+2H2O,先产生沉淀,然后沉淀消失,两次消耗的氢氧化钠的物质的量都为0.02mol(即20mLNaOH溶液),产生的Be(OH)2沉淀为0.01mol,沉淀量随NaOH溶液加人量的变化图为: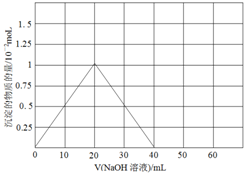 ;
;
故答案为:BeO+2H+=Be2++H2O; ;
;
(2)①GeCl4与水反应生成GeO2和氯化氢,方程式为:GeCl4+2H2O=GeO2+4HCl;
故答案为:GeCl4+2H2O=GeO2+4HCl;
②A.GeO2与SiO2性质不相似,GeO2与盐酸反应,SiO2与盐酸不反应,故A错误;
B.过程Ⅱ的蒸馏是利用GeCl4的沸点低来实现的,不是利用GeCl4难溶于水的性质实现的,故B错误;
C.过程Ⅳ发生的反应中,GeO2中Ge的化合价降低,作氧化剂,故C正确;
D.过程Ⅰ、Ⅲ是复分解反应,过程Ⅳ是置换反应,属于氧化还原反应,故D正确;
故答案为:CD;
(3)将硫与浓硝酸混合,结果生成一种纯净无色气体A,A遇空气变红棕色,说明A为一氧化氮,由于浓硝酸的强氧化性,能将硫氧化成+6价的硫酸,化学方程式为:S+2HNO3=H2SO4+2NO↑;
故答案为:S+2HNO3=H2SO4+2NO↑.
点评 本题主要考查了同主族元素性质的相似性和差异性,注意根据题意提取信息是解题的关键,题目难度中等.


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②④⑤⑥ | C. | ①②④ | D. | ①②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
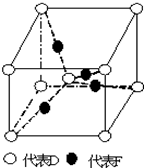 在周期表中1~36号之间的A、B、C、D、E、F六种元素,它们的原子序数依次增大,已知A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C元素原子的最外层有3个自旋方向相同的未成对电子,D原子核外电子有8种不同的运动状态,E元素在第四周期,E的基态原子中未成对电子数是核外电子总数的$\frac{1}{4}$,F元素位于周期表的ds区,其基态原子最外能层只有一个电子.
在周期表中1~36号之间的A、B、C、D、E、F六种元素,它们的原子序数依次增大,已知A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C元素原子的最外层有3个自旋方向相同的未成对电子,D原子核外电子有8种不同的运动状态,E元素在第四周期,E的基态原子中未成对电子数是核外电子总数的$\frac{1}{4}$,F元素位于周期表的ds区,其基态原子最外能层只有一个电子. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(B)=1.5 mol•L-1•min-1 | B. | v(B)=3 mol•L-1•min-1 | ||
| C. | v(D)=2 mol•L-1•min-1 | D. | v(C)=1 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
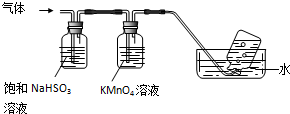
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
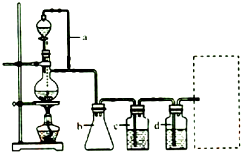

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
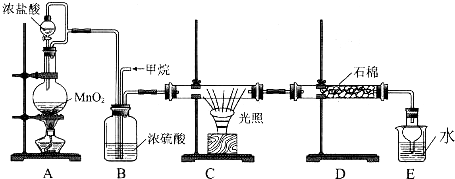
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某化合物焰色反应呈黄色,说明该物质中一定含有Na+ | |
| B. | 向某溶液中加入盐酸有气泡产生,说明一定有CO32- | |
| C. | 向某溶液中加入氯化钡溶液,有白色沉淀产生,说明一定有SO42- | |
| D. | 向某溶液中加入硝酸银溶液,有白色沉淀产生,说明一定有Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com