

分析 同种物质组成的为纯净物,不同物质组成的为混合物;
同种元素组成的纯净物为单质,不同元素组成的纯净物为化合物;
根据酸是水溶液中电离出的阳离子全部是H+的化合物;
碱是水溶液中电离出的阴离子全部是OH-离子的化合物;
盐是电离出阳离子是金属阳离子或铵根离子、阴离子为酸根离子的化合物;
氧化物由两种元素组成,其中一种为氧元素的化合物;
分散质粒子的直径大小在1nm~100nm的是胶体,分散质粒子的直径大于100nm的是浊液,分散质粒子的直径小于1nm的是溶液.
解答 解:A.水银为金属汞,是由汞元素组成的单质;
B.纯碱的化学式为Na2CO3,由金属阳离子和酸根离子构成的盐;
C.豆浆分散质粒子的直径大小在1nm~100nm,属于胶体;
D.盐酸是氯化氢气体的水溶液,属于混合物;
E.泥水是由泥和水形成的浊液.
F.H2SO4在水溶液中电离出的阳离子全部是H+属于酸;
G.氢氧化钠固体水溶液中电离出的阴离子全部是OH-,属于碱;
H.水是由两种元素组成,其中一种为氧元素的化合物,属于氧化物;
I.二氧化碳是由两种元素组成,其中一种为氧元素的化合物,属于氧化物;
溶液有D,豆浆为胶体,浊液为E,单质为A,酸为F,碱为G,盐为B,氧化物为H、I,
故答案为: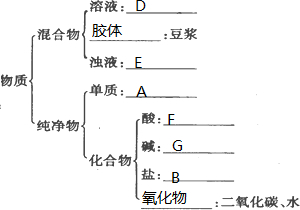 .
.
点评 本题考查酸碱盐以及氧化物、胶体的概念及分类,题目难度不大,解答本题的关键是理解相关概念以及物质的组成和俗称,注意知识的积累.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 增加Ni的量可提高CO的转化率,Ni的转化率降低 | |
| B. | 缩小容器容积,平衡右移,△H减小 | |
| C. | 反应达到平衡后,充入CO再次达到平衡时,CO的体积分数降低 | |
| D. | 当4v正[Ni(CO)4]=v正(CO)时或容器中混合气体密度不变时,都可说明反应已达化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
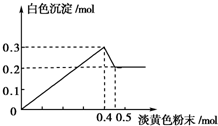 有一透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一种淡黄色粉末固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀.当加入0.4mol淡黄色粉末时,产生气体0.3mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如如图所示.(已知:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O).
有一透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一种淡黄色粉末固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀.当加入0.4mol淡黄色粉末时,产生气体0.3mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如如图所示.(已知:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属铝投入NaOH溶液中:2Al+2OH-+H2O═2AlO2-+2H2↑ | |
| B. | 石英与烧碱反应:SiO2+2OH-═SiO32-+H2O | |
| C. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 向小苏打溶液中加入过量Ba(OH)2:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用HNO3除去铜粉中混杂的Zn | |
| B. | 通入Cl2,除去Fe2(SO4)3溶液中的FeSO4 | |
| C. | 通过饱和食盐水,除去Cl2中的HCl | |
| D. | 通过饱和Na2CO3溶液,除去CO2中的SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光导纤维是信息社会必不可少的有机合成材料 | |
| B. | 食盐加碘实质是在食盐中加入KIO3 | |
| C. | 航天飞机上的陶瓷防护片属于新型无机非金属材料 | |
| D. | 焚烧垃圾会产生大量污染空气的物质,故不宜采用此法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
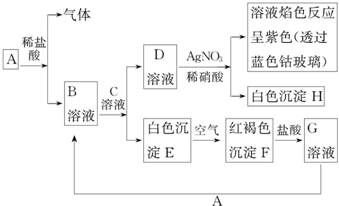
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
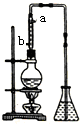 分液.
分液.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com