




| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
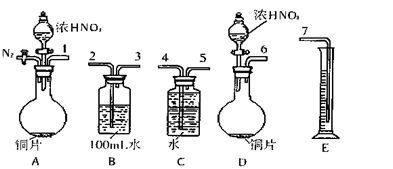
| A��V��NO2��: V��O2��= 4 : 1 |
| B��V��NO2��: V��NO��= 1 : 0 |
| C��V��NO2��: V��NO��= 1 : 2 |
| D��V��NO2��: V��NO��: V��O2��=" 1" : 1 : 1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������������ˮ | B������ˮ��Һ���Ժ�ǿ |
| C���������л�ԭ�� | D��һˮ�ϰ��ܲ��ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
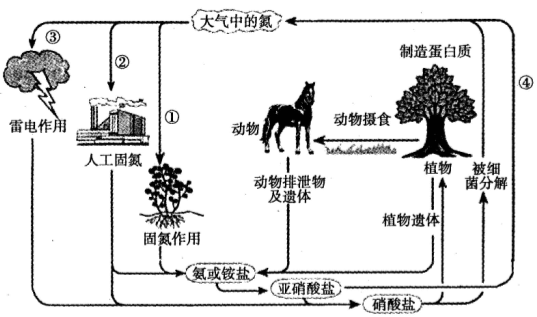
| A���٢� | B���ۢ� | C���٢� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NH3��Һ����Һ������������� |
| B������ȶ������Ȼ�����ֽ� |
| C�����������ֽ⣬������氱̬����ʱҪ�ܷⱣ�棬����������ͨ�紦 |
| D��ϡ����ͻ��ý�����Ӧʱ��Ҫ�õ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����³�ѹ�£�һ��������������е�����ֱ�ӻ��� |
| B��һ��������Ħ������Ϊ30 |
| C��һ��������һ�ֺ���ɫ������ |
| D��һ������������ˮ����������ˮ���ռ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com