
下列叙述中正确的是( )
A.将KI和FeCl3溶液棍合,溶液变棕黄色,说明还原性Fe2+>I-
B.NO2通入FeSO4溶液中的过程中由浅绿色变为黄色
C.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2
D.SO2通入BaCl2溶液中先有白色沉淀后沉淀溶解
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届江西省高三全真模拟理综化学试卷(解析版) 题型:填空题
铁是一种过渡元素,金属铁是最常用的金属。请回答下列各题:
(1)生铁中含有一种铁碳化合物(Fe3C),在足量的空气中高温煅烧,生成有磁性的固体和能使澄清石灰水变浑浊的气体,该反应的化学方程式为 。上述反应生成的磁性固体能溶于过量盐酸,该反应的离子方程式为 。
(2)在Fe2+或Fe3+的催化作用下,可实现2SO2+O2+2H2O=2H2SO4的转化。已知含SO2的废气通入含Fe2+的溶液时,其中一个反应的离子方程式为2Fe3+ + SO2 + 2H2O = 2Fe2+ + SO42- + 4H+,则另一反应的离子方程式为 。
(3)硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制绿矾。利用烧渣制绿矾的过程如下:
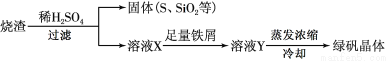
①烧渣溶于稀H2SO4过程中,先是固体大部分被溶解,接着有单质硫生成,写出该反应的离子方程式(只写生成S的离子方程式,其他反应无需写出) 。
②向溶液X中加入足量铁屑的目的是 。
③取1.6g所得晶体样品配成溶液,滴入 mL 0.1000 mol/L 的酸性高锰酸钾液刚好完全反应,经计算可得样品中含47.5%的硫酸亚铁。
(4)已知Fe(OH)3的溶度积常数Ksp=1.1×10-36。室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH=3时,通过计算说明Fe3+是否沉淀完全 。
(提示:当某离子浓度小于1.0×10-5 mol•L-1时可以认为该离子沉淀完全了)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一下期中化学试卷(解析版) 题型:选择题
某主族元素R的原子的电子式可表示为: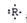 ;该元素组成的以下物质,其化学式肯定错误的是( )
;该元素组成的以下物质,其化学式肯定错误的是( )
A.最高价氧化物分子式为R2O5 B.含氧酸分子式为HRO3
C.含氧酸分子式为H3RO4 D.气态氢化物分子式为RH5
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中理科化学试卷(解析版) 题型:填空题
向含有Mg2+、Fe2+、Al3+、NH4+四种离子的溶液中加入过量的NaOH溶液,微热并搅拌(考虑空气中的氧气氧化作用),再加入过量的盐酸后,上述阳离子大量减少的是_________,加入盐酸之前溶液中发生反应的所有离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中理科化学试卷(解析版) 题型:选择题
将浓度为0.1mol•L-1HF溶液加水不断稀释,下列各量始终保持增大的是( )
A.c(H+) B.Ka(HF) C.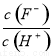 D.
D.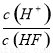
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中理科化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关,下列说法正确的是( )
A.小苏打用于治疗胃溃疡病人的胃酸过多症
B.工厂常用的静电除尘方法与胶体性质无关
C.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板
D.电解从海水中得到的氯化钠溶液可获得金属钠
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中理科化学试卷(解析版) 题型:选择题
对相同状况下的12C18O和14N2两种气体,下列说法正确的是
A.若质量相等,则质子数相等
B.若原子数相等,则中子数相等
C.若分子数相等,则体积相等
D.若体积相等,则密度相等
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下期中化学试卷(解析版) 题型:选择题
高分子化合物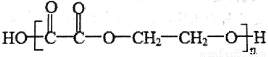 ,可由有机化工原料R和其他有机试剂,通过卤化、水解、氧化、缩聚反应得到,则R是( )
,可由有机化工原料R和其他有机试剂,通过卤化、水解、氧化、缩聚反应得到,则R是( )
A.1-丁烯 B.乙炔 C.1, 3-丁二烯 D.乙烯
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三5月模拟考试理综化学试卷(解析版) 题型:实验题
某学习小组研究溶液中Fe2+的稳定性;进行如下实验,观察,记录结果。
实验I
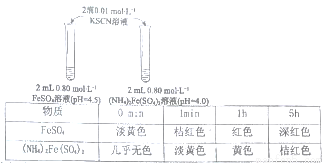
(1)上述(NH4)2Fe(SO4)2溶液pH小于FeSO4的原因是_____________(用化学用语表示)。溶液的稳定性:FeSO4_______(NH4)2Fe(SO4)2(填“>”或“<”)。
(2)甲同学提出实验I中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+有还原性,进行实验Ⅱ,否定了该观点,补全该实验。

(3)乙同学提出实验I中两溶液的稳定性差异是溶液酸性不同导致,进行实验Ⅲ;分别配制0.80mol•L-1pH为1、2、3、4的FeSO4溶液,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短。
资料显示:亚铁盐溶液中存在反应 4Fe2++O2+10H2O 4Fe(OH)3+8H+ 由实验Ⅲ,乙同学可得出的结论是_________,原因是_________。
4Fe(OH)3+8H+ 由实验Ⅲ,乙同学可得出的结论是_________,原因是_________。
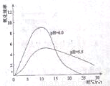
(4)进一步研究在水溶液中Fe2+的氧化机理,测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如图(实验过程中溶液温度几乎无变化)。反应初期,氧化速率逐渐增大的原因可能是_________。
(5)综合以上实验,增强Fe2+稳定性的措施有_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com