
【题目】下表是不同温度下水的离子积数据:
温度/℃ | 25 | t1 | t2 |
水的离子积常数 | 1×10-14 | α | 1×10-12 |
试回答以下问题:
(1)若25<t1<t2,则α__(填“<”“>”或“=”)1×10-14,作出此判断的理由是___。
(2)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4mol·L-1,取该溶液1mL,加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=___。
(3)t2℃下,将pH=11的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=___。
【答案】> 升高温度,水的电离程度增大,离子积增大 1000∶1 9∶11
【解析】
(1).水的电离是吸热的,所以升温促进水的电离,电离平衡常数增大,即α>1×10-14;
(2) Na2SO4溶液中c(SO42-)=5×10-4mol·L-1,则钠离子浓度为10-3 mol·L-1,加水稀释,钠离子浓度变为10-4 mol·L-1,溶液中的氢氧根离子浓度为10-7 mol·L-1,二者比例为10-4:10-7=1000∶1;
(3) t2℃下,将pH=11的苛性钠溶液V1L氢氧根离子浓度为10-1 mol·L-1,与pH=1的稀硫酸V2L中氢离子浓度为10-1 mol·L-1,混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2 ,则有![]() ,解V1:V2=9∶11。
,解V1:V2=9∶11。


科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入0.3molA、0.1molC和一定量B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示[t0~t1阶段c(B)未画出]。图乙为t2时刻后改变条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种条件并且所用条件均不相同。已知t3~t4阶段为使用催化剂。下列说法正确的是( )
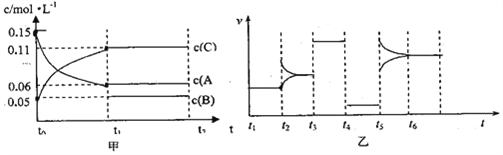
A. 若t1等于15s,生成物C在t0~t1时间段的平均反应速率为0.004mol/(Ls)
B. t4~t5阶段改变的条件为降低反应温度
C. B的起始的物质的量为0.02mol
D. t5~t6阶段可能是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
A. 一定温度下,反应2H2(g)+O2(g) ![]() 2H2O(g)能自发进行,该反应的ΔH<0
2H2O(g)能自发进行,该反应的ΔH<0
B. 氢氧燃料电池的负极反应为O2+2H2O+4e![]() 4OH
4OH
C. 常温常压下,氢氧燃料电池放电过程中消耗11.2 L H2,转移电子的数目为6.02×1023
D. 反应2H2(g)+O2(g) ![]() 2H2O(g)的ΔH可通过下式估算:
2H2O(g)的ΔH可通过下式估算:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在其他条件不变时,只改变某一条件,化学反应aA(g)+B(g)![]() cC(g)的平衡的变化图象如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是
cC(g)的平衡的变化图象如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是

A. 在图象反应Ⅰ中,说明正反应为吸热反应
B. 在图象反应Ⅰ中,若p1>p2,则此反应的ΔS>0
C. 在图象反应Ⅱ中,说明该正反应为吸热反应
D. 在图象反应Ⅲ中,若T1>T2,则该反应能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在80℃时,将0.40 mol的四氧化二氮气体充入2 L的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4)/mol·L-1 | 0.20 | a | 0.10 | c | d | e |
c(NO2)/mol·L-1 | 0.00 | 0.12 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)该反应的化学方程式为________________________。
(2)该反应在0~20 s内N2O4的平均反应速率为____________。
(3)在80℃时该反应的平衡常数K值为______________。
(4)在20s时,浓度熵Qc_________(填“>”、“<”或“=”)平衡常数K。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)下列关于金属及金属键的说法不正确的是______。(填字母代号)
a.金属键没有方向性与饱和性
b.金属键是金属原子与自由电子间的相互作用
c.金属熔沸点不同的原因可以用金属键强弱解释
d.电子气理论可解释金属材料的延展性,不能解释金属有良好的导电性
(2)钒广泛用于催化及钢铁工业,基态钒原子的价层电子排布图为_________________。
(3)二茂铁又叫双环戊二烯基铁[Fe(C5H5)2],熔点是172.5~173 ℃,100 ℃以上升华,二茂铁属于_____晶体。已知分子中的大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为![]() )。已知二茂铁的每个茂环带有一个单位负电荷,则每个环中的大π键应表示为________________。
)。已知二茂铁的每个茂环带有一个单位负电荷,则每个环中的大π键应表示为________________。
(4)铜可以形成一种离子化合物[Cu(NH3)4(H2O)2]SO4,若要确定[Cu(NH3)4(H2O)2]SO4是晶体还是非晶体,最科学的方法是对其进行______实验,其中阴离子的空间构型是_____,该化合物加热时首先失去的组分是H2O,原因是_______________________。
(5)最近发现,只含镁、镍和碳三种元素的晶体也具有超导性,该物质形成的晶体的立方晶胞结构如图所示。
①与Mg紧邻的Ni有________个。
②原子坐标参数可表示晶胞内部各原子的相对位置。该晶胞中原子的坐标参数为a为(0,0,0);b为(1/2,1/2,0);d为(1,1,1)。则c原子的坐标参数为_______。
③若晶胞中Ni、Mg之间的最短距离为a pm,阿伏加德罗常数的值为NA,则晶体的密度ρ=______g·cm-3(用含a、NA的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】给格列汀![]()

![]() 是用于治疗2型糖尿病的药物,工业上以烃A为基本原料合成给格列汀的过程如下。
是用于治疗2型糖尿病的药物,工业上以烃A为基本原料合成给格列汀的过程如下。
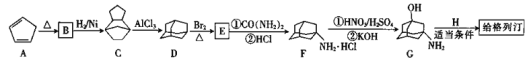
已知:![]()
![]() 的分子式是__________,A生成B的反应类型为______________。
的分子式是__________,A生成B的反应类型为______________。
![]() 中所含官能团的名称为__________。
中所含官能团的名称为__________。
![]() 给格列汀
给格列汀![]() ,则H的结构简式为______,C、D不可能_____
,则H的结构简式为______,C、D不可能_____![]() 填字母
填字母![]() 。
。
![]() 互为同分异构体
互为同分异构体 ![]() 互为同系物
互为同系物 ![]() 是环烷烃
是环烷烃 ![]() 发生氧化反应
发生氧化反应
![]() 写出D生成E的化学方程式:_____________________。
写出D生成E的化学方程式:_____________________。
![]() 有许多同分异构体,其中分子中含有两种官能团的同分异构体共有______种,写出一种核磁共振氢谱图中有4个峰的物质的结构简式:_________。
有许多同分异构体,其中分子中含有两种官能团的同分异构体共有______种,写出一种核磁共振氢谱图中有4个峰的物质的结构简式:_________。
![]() 写出以
写出以![]() 丁烯为原料合成重要的有机合成中间体
丁烯为原料合成重要的有机合成中间体![]()
![]()
![]() 的流程路线图
的流程路线图![]() 无机试剂任选
无机试剂任选![]() ____________
____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】屈昔多巴( )可治疗直立性低血压所致头昏、头晕和乏力,帕金森病患者的步态僵直等。以下是屈昔多巴的一种合成路线(通常
)可治疗直立性低血压所致头昏、头晕和乏力,帕金森病患者的步态僵直等。以下是屈昔多巴的一种合成路线(通常![]() 简写为BnCl,
简写为BnCl,![]() 简写为CbzCl ):
简写为CbzCl ):

回答下列问题:
(1)反应①的反应类型为_____________,其作用为_________________。
(2)屈昔多巴中所含的非含氧官能团名称为_______________,屈昔多巴分子中有___________个手性碳原子。
(3)反应②为加成反应,有机物X的名称为______________________。
(4)![]() 显________________性(填“酸”、“中”或“碱”),写出其与盐酸反应的化学方程式:_______________________。
显________________性(填“酸”、“中”或“碱”),写出其与盐酸反应的化学方程式:_______________________。
(5)![]() 的同分异构体中,能与NaHCO3溶液反应生成CO2的二取代芳香化合物有_______种,其中核磁共振氢谱为四组峰的结构简式为______________(任写一种)。
的同分异构体中,能与NaHCO3溶液反应生成CO2的二取代芳香化合物有_______种,其中核磁共振氢谱为四组峰的结构简式为______________(任写一种)。
(6)参照上述合成路线,以对羟基苯甲醛为原料(无机试剂任选),设计制备对羟基苯甲酸的合成路线:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生态溶液涉及农家肥料的综合利用,某种肥料经发酵得到一种含有甲烷、二氧化碳、氮气的混合气体。2.016L(标准状况)该气体通过盛有红色CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO![]() CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。
CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。
(1)原混合气体中甲烷的物质的量是____________。
(2)原混合气体中氮气的体积分数为多少?(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com