
分析 (1)反应后得到只含一种金属阳离子的浅绿色溶液和1.28g固体铜,说明反应后恰好生成硫酸亚铁,氧化铜完全转化成铜单质,根据n=$\frac{m}{M}$计算出1.28gCu的物质的量,然后根据铜元素守恒得出CuO的物质的量,再根据m=nM计算出CuO的质量,然后根据混合物总质量计算出铁粉的质量,再结合n=$\frac{m}{M}$计算出计算出该样品中铁粉和氧化铜的物质的量之比;
(2)根据硫酸根离子守恒可得出硫酸的物质的量,然后根据c=$\frac{n}{V}$计算出硫酸的浓度;根据电子守恒计算出生成氢气的物质的量,再根据V=nVm计算出产生H2在标准状况下的体积.
解答 解:(1)铁粉和氧化铜混合均匀的粉末样品4.40g,加入50mL稀硫酸恰好充分反应后,得到只含一种金属阳离子的浅绿色溶液和1.28g固体铜,说明反应后溶质为硫酸亚铁,CuO中的铜元素完全反应转化成Cu单质,1.28g铜的物质的量为:$\frac{1.28g}{64g/mol}$=0.02mol,根据铜元素质量守恒可知原混合物中CuO的物质的量为0.02mol,质量为:80g/mol×0.02mol=1.6g,则原混合物中铁粉的质量为:4.4g-1.6g=2.8g,铁粉的物质的量为:$\frac{2.8g}{56g/mol}$=0.05mol,所以该样品中铁粉和氧化铜的物质的量之比=0.05mol:0.02mol=5:2,
故答案为:0.02;5:2;
(2)反应后溶质为硫酸亚铁,硫酸恰好反应,根据硫酸根离子守恒可知50mL稀硫酸中含有硫酸的物质的量为:n(H2SO4)=n(FeSO4)=n(Fe)=0.05mol,该稀硫酸的浓度为:c(H2SO4)=$\frac{0.05mol}{0.05L}$=1.0mol/L;
根据(1)可知原混合物中含有0.05molFe、0.02molCuO,根据根据电子守恒可知:2n(Fe)=2n(H2)+2n(CuO),则n(H2)=0.05mol-0.02mol=0.03mol,标准状况下0.03mol氢气的体积为:22.4L/mol×0.03mol=0.672L,
故答案为:1.0;0.672.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
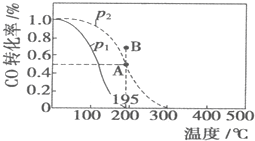 在20L恒容密闭容器中,按物质的量之比为1:2充入CO和H2发生:CO(g)+2H2(g)?CH3OH(g)△H=akJ/mol.测得CO的转化率随温度及不同压强的变化如图所示:n(H2)在P2及195℃时随时间变化如表所示
在20L恒容密闭容器中,按物质的量之比为1:2充入CO和H2发生:CO(g)+2H2(g)?CH3OH(g)△H=akJ/mol.测得CO的转化率随温度及不同压强的变化如图所示:n(H2)在P2及195℃时随时间变化如表所示| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8 | 5 | 4 | 4 |
| A. | P1>P2,a<0 | |
| B. | 在P2及195℃时,反应前3min的平均速率v(CH3OH)=0.08mol/(L•min) | |
| C. | 在P2及195℃时,该反应的平衡常数为25(mol/L)-2 | |
| D. | 在B点时,v正>v逆 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3=Na++H++CO32- | B. | Fe2(SO4)3=2Fe3++3SO42- | ||
| C. | MgCl2=Mg2++2Cl- | D. | NaOH=Na++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 编号 | 0.01mol•L-1 酸性KMnO4溶液 | 0.1mol•L-1 H2C2O4溶液 | 水 | 1mol•L-1 MnSO4溶液 | 反应温度 /℃ | 反应时间 |
| Ⅰ | 2mL | 2mL | 0 | 0 | 20 | 125 |
| Ⅱ | v1mL | v2mL | 1mL | 0 | 20 | 320 |
| Ⅲ | v3mL | v4mL | v5mL | 0 | 50 | 30 |
| Ⅳ | 2mL | 2mL | 0 | 2滴 | 20 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和反应的反应热测定需用温度计测量温度二次,分别为反应的起始温度和最高温度 | |
| B. | 用试纸检验气体时,可先把试纸用蒸馏水润湿,粘在玻璃棒一端,用玻璃棒把试纸放到盛待测气体的容器口附近 | |
| C. | 用剩的药品能否放回原瓶,应视具体情况而定 | |
| D. | 将铂丝放在盐酸中洗涤并灼烧为无色后,再蘸取待测物进行焰色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | SO2通入BaCl2溶液,然后滴入稀硝酸 | 有白色沉淀,白色沉淀不溶于稀硝酸 | 所得沉淀为BaSO3,后转化为BaSO4 |
| B | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| C | 将稀硫酸滴入碳酸钠溶液中产生的气体通入硅酸钠溶液 | 有白色沉淀生成 | 证明非金属性S>C>Si |
| D | 向含有淀粉的FeI2溶液中滴加足量的氯水 | 溶液变蓝 | 还原性:I->Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 操作 | |
| A | 证明某溶液中存在Fe2+ | 先加少量氯水,再滴加KSCN溶液,出现血红色 |
| B | 测定熔融苛性钠的导电性 | 在瓷坩埚中熔化氢氧化钠固体后进行测量 |
| C | 证明氯的非金属性大于碳 | 向碳酸钙中滴加盐酸,有气泡产生 |
| D | 制备氯化镁晶体 | 将MgCl2溶液在氯化氢的气流中蒸干 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
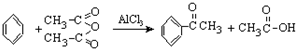
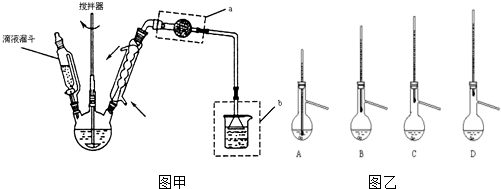
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com