

 .
.分析 (1)N2H4、H2O2分子中N、H、O三种元素,氧元素的电负性最大,同周期从左向右第一电离能增大,从上向下第一电离能减小,据此答题;
(2)钛的原子序数为22,根据核外电子排布规律画出电子排布式示意图;
(3)N2H4分子中氮氮之间有一个共价键,氮氢之间都有共价键,据此判断共价键数目;
(4)根据H2O2分子中氧原子的价层电子对数判断其中心原子杂化方式,根据相似相溶原理答题;
(5)根据氮化硼晶胞图判断处于晶胞顶点上的原子的配位数,根据V=$\frac{m}{ρ}$计算晶胞的体积,进而确定晶胞的边长,晶体N原子位于晶胞体对角线的 $\frac{1}{4}$处,将体心与下底面相对的两顶点相连可构成等腰三角形,距离最近的两个N原子相连的连线为该三角形的中位线,所以晶体中最近的两个N原子的距离为底面对角线的一半.
解答 解:(1)N2H4、H2O2分子中N、H、O三种元素,氧元素的电负性最大,位于周期表中第二周期第ⅤⅠA族,同周期从左向右第一电离能增大,从上向下第一电离能减小,所以第一电离能最大的元素为N,
故答案为:第二周期第ⅤⅠA族;N;
(2)钛的原子序数为22,核外电子排布式示意图为 ,
,
故答案为: ;
;
(3)N2H4分子中氮氮之间有一个共价键,氮氢之间都有共价键,所以1mol N2H4分子中含有的共价键数目为3.01×1024,
故答案为:3.01×1024;
(4)根据H2O2分子中氧原子的价层电子对数为$\frac{6+1+1}{2}$=4,所以氧原子杂化方式为sp3,H2O2为极性分子,CS2为非极性溶剂,根据相似相溶原理,H2O2不能溶解在CS2中,
故答案为:sp3;H2O2为极性分子,CS2为非极性溶剂,所以H2O2不能溶解在CS2中;
(5)根据图知,顶点上的每个B原子和四个N原子形成共价键,所以B原子的配位数是4;该晶胞中N原子个数是4,B个数=$\frac{1}{8}$×8+6×$\frac{1}{2}$=4,晶胞体积=$\frac{\frac{4M}{{N}_{A}}}{ρ}$=$\frac{100}{{N}_{A}ρ}$cm3,晶胞边长=$\root{3}{\frac{100}{N{\;}_{A}ρ}}$cm,晶胞底面对角线长=$\sqrt{2}×\root{3}{\frac{100}{{N}_{A}ρ}}$cm,晶体N原子位于晶胞体对角线的 $\frac{1}{4}$处,将体心与下底面相对的两顶点相连可构成等腰三角形,距离最近的两个N原子相连的连线为该三角形的中位线,所以晶体中最近的两个N原子的距离为底面对角线的一半,所以两个最近N原子间的距离=$\frac{\sqrt{2}}{2}×\root{3}{\frac{100}{{N}_{A}ρ}}$cm,
故答案为:4;$\frac{\sqrt{2}}{2}×\root{3}{\frac{100}{{N}_{A}ρ}}$.
点评 本题是对物质结构的考查,涉及核外电子排布、杂化轨道、物质的性质、晶胞结构与计算等,需要学生具备扎实的基础,难度中等.


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:选择题
| A. | NaOH | B. | NaCl | C. | H2O | D. | Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)2CHCH2CH2CH3 | B. | (CH3CH2)2CHCH3 | C. | (CH3)2CBrCH(CH3)2 | D. | (CH3)2CHCH2CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
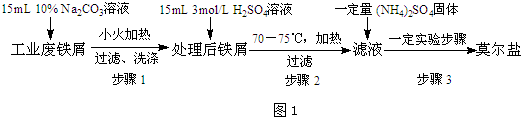
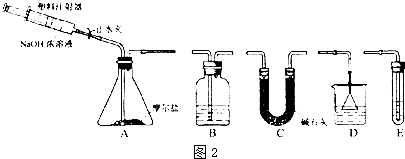
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫铁矿高温下被空气氧化产生二氧化硫:4FeS2+11O2→8SO2+2Fe2O3.设空气中N2、O2的含量分别为0.800和0.200(体积分数,以下气体含量均用体积分数表示),试完成下列各题:
硫铁矿高温下被空气氧化产生二氧化硫:4FeS2+11O2→8SO2+2Fe2O3.设空气中N2、O2的含量分别为0.800和0.200(体积分数,以下气体含量均用体积分数表示),试完成下列各题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 石灰水、裂化汽油 | B. | NaHS溶液、SO2 | ||
| C. | NaCl溶液、NaI溶液 | D. | CaCl2溶液、Na2S溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体A为SO2 | B. | 反应中共消耗Zn 97.5 g | ||
| C. | 气体A中SO2和H2的体积比为4:1 | D. | 反应中共转移3 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液的pH=4 | |
| B. | 由HA电离出的c(H+)约为水电离出的c(H+)的106倍 | |
| C. | 在该温度下加水稀释,溶液中$\frac{c({H}^{+})}{c(HA)}$减小 | |
| D. | 此酸的电离平衡常数约为1.0×10-7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com