
| A. | 标准状况下,1molSO3的气体体积为22.4L | |
| B. | 1mol铁粉与过量Cl2反应时,转移电子数为2NA | |
| C. | 含有2NA个氧原子的D2O质量为40g | |
| D. | 16gO2分子中含有的氧原子数为0.5NA |
分析 A、标况下三氧化硫为固体;
B、铁和氯气反应后变为+3价;
C、一个重水分子含1个氧原子,故含2NA个氧原子的重水为2mol;
D、氧气由氧原子构成.
解答 解:A、标况下三氧化硫为固体,故不能根据气体摩尔体积来计算其体积,故A错误;
B、铁和氯气反应后变为+3价,故1mol铁反应后转移3NA个电子,故B错误;
C、一个重水分子含1个氧原子,故含2NA个氧原子的重水为2mol,而重水的摩尔质量为20g/mol,故2mol重水的质量为40g,故C正确;
D、氧气由氧原子构成,故16g氧气中含1mol氧原子即NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 仅用新制氢氧化铜悬浊液(可以加热)不能通过化学方法完成对葡萄糖溶液、乙醇和乙酸溶液的鉴别 | |
| B. | 利用加碳酸钠饱和溶液和分液的方法可以除去乙酸乙酯中的乙酸和乙醇 | |
| C. | CH3CH2CH2OH和CH3CH2CH2Cl的同分异构体数目相同 | |
| D. | 石油的分馏、裂化,煤的干馏,都是通过化学变化获得新物质的工业生产方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1s | B. | 2.5s | C. | 5s | D. | 10s |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O (l)△H=+1135.7kJ•mol-1 | |
| B. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(l)△H=-1135.7kJ•mol-1 | |
| C. | N2H4(g)+NO2(g)═N2(g)+2H2O(g)△H=+1135.7kJ•mol-1 | |
| D. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g)△H=-1135.7kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | 只有①④ | C. | 只有①③④ | D. | 只有①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水或熔融氯化钠时,阳极的电极反应式均为2Cl--2e-═Cl2↑ | |
| B. | 钢铁发生吸氧腐蚀和析氢腐蚀的负极反应式均为Fe-2e-═Fe2+ | |
| C. | 精炼铜和电镀铜时,与电源负极相连的电极反应式均为Cu2++2e-═Cu | |
| D. | 酸性介质或碱性介质的氢氧燃料电池的正极反应式均为O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
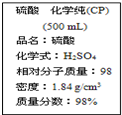
| A. | 该硫酸的物质的量浓度为18.4 mol/L | |
| B. | 该硫酸常用做干燥剂 | |
| C. | 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL | |
| D. | 该硫酸与等质量的水混合后所得溶液的浓度大于9.2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成H2的质量为0.01g | |
| B. | 生成的H2中含有的氢原子数为1.204×l023个 | |
| C. | 生成H2的体积为0.112L(以标准状况) | |
| D. | 生成H2的物质的量为0.01mol |
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上定时训练8化学卷(解析版) 题型:选择题
下列有关仪器的性能或者使用方法的说明中正确的是
A.试管、蒸发皿既能用于给固体加热也能用于给溶液加热
B.分液漏斗既能用于某些混合物的分离也能用于组装气体发生器
C.碱式滴定管既可用于中和滴定,也可用于量取一定量的NaCl或AlCl3溶液
D.测量酒精沸点的实验中,应使温度计水银球位于被加热的酒精中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com