
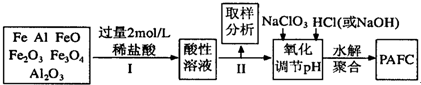
分析 Al、Fe单质及其氧化物中加入稀盐酸得到酸性溶液,酸性溶液加入NaClO3,发生氧化反应,再调节pH、水解、聚合得到[AlFe(OH)nCl6-n]m,
(1)根据配制一定物质的量浓度的溶液的步骤选择使用的仪器;
(2)A.酸性条件下NaClO3可将Fe2+生成Fe3+;
B.不属于高分子化合物;
C.该物质可以电离出氯离子,不属于碱;
D.氢氧化铝能与强酸、强碱反应;
(3)步骤Ⅱ中取样分析的目的是测定溶液中Fe2+的含量,以确定加入NaClO3 的量;
(4)氯酸钠氧化酸性的氯化亚铁,则反应物中有氢离子参加,则生成物中有水生成,Cl元素的化合价从+5价降低到-1价,得到6个电子,而Fe元素的化合价从+2价升高到+3价,失去1个电子,根据得失电子守恒,则氯酸根离子的系数为1,Fe2+的系数为6,则铁离子的系数也是6,氯离子的系数是1,根据电荷守恒,则氢离子的系数是6,水的系数是3;
(5)氢氧化铝溶液氢氧化钠溶液,氢氧化铁不溶液氢氧化钠溶液,利用碳酸酸性大于氢氧化铝,二氧化碳通入偏铝酸钠溶液中生成氢氧化铝沉淀,利用沉淀质量进行Fe、Al的测定;
(6)为测定产品PAFC中A1和Fe的含量,取一定量产品溶于氢氧化钠溶液中过滤得到氢氧化铁沉淀,灼烧得到氧化铁,冷却称量,滤液中通入二氧化碳得到氢氧化铝沉淀,过滤洗涤,灼烧分解得到氧化铝称量,然后分别计算铁、铝的含量;
(7)依据(6)分析可知灼烧得到固体为氧化铝和氧化铁.
解答 解:(1)浓盐酸配制一定物质的量浓度的稀盐酸,所用玻璃仪器除量筒和玻璃棒外,还有烧杯、容量瓶,故选AB,
故答案为:AB;
(2)A.PAFC(聚合氯化铁铝[AlFe(OH)nC16-n]m),属于无机高分子化合物,故A正确;
B.酸性条件下NaClO3可将Fe2+生成Fe3+,该物质中Fe元素的化合价为+3,故B错误;
C.该物质可以电离出氯离子,不属于碱,故C错误,
D.氢氧化铝能与强酸、强碱反应,该物质在强酸和强碱性溶液中均不能稳定存在,故D正确;
故答案为:AD;
(3)酸性溶液中取样分析溶液中含有亚铁离子的含量,用来确定加入NaClO3的量,用来氧化亚铁离子为铁离子,
故答案为:C;
(4)氯酸钠氧化酸性的氯化亚铁,则反应物中有氢离子参加,则生成物中有水生成,Cl元素的化合价从+5价降低到-1价,得到6个电子,而Fe元素的化合价从+2价升高到+3价,失去1个电子,根据得失电子守恒,则氯酸根离子的系数为1,Fe2+的系数为6,则铁离子的系数也是6,氯离子的系数是1,根据电荷守恒,则氢离子的系数是6,水的系数是3,配平后离子方程式为:6Fe2++6H++ClO3-=6Fe3++Cl-+3H2O;
故答案为:6,6,1,6,1,3;
(5)测定产品PAFC中A1和Fe的含量,取一定量产品溶于氢氧化钠溶液中过滤得到氢氧化铁沉淀,灼烧得到氧化铁,冷却称量,滤液中通入二氧化碳得到氢氧化铝沉淀,过滤洗涤,灼烧分解得到氧化铝称量,需要的试剂为氢氧化钠溶液和二氧化碳,选BC,
故答案为:B C;
(6)取一定量产品溶于氢氧化钠溶液中过滤得到氢氧化铁沉淀,灼烧得到氧化铁,冷却称量,滤液中通入二氧化碳得到氢氧化铝沉淀,过滤洗涤,灼烧分解得到氧化铝称量,
故答案为:洗涤;冷却;
(7)分析可知测定时,通过灼烧后等操作,直接测定的是Al2O3,Fe2O3 的质量,
故答案为:Al2O3;Fe2O3.
点评 本题考查了铁的化合物性质的应用、氧化还原反应方程式的配平、平衡移动影响因素等,需要学生具备扎实的基础与灵活运用难度,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 质子数为1 | B. | 电子数为3 | C. | 中数为2 | D. | 质量数为3 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯属于不饱和链烃,乙烷属于饱和链烃 | |
| B. | 乙烯分子中所有原子处于同一平面上,乙烷分子则为立体结构,所有原子不在同一平面上 | |
| C. | 乙烯分子中的双键和乙烷分子中的单键相比较,双键的键能大,键长长 | |
| D. | 乙烯能使酸性KMnO4溶液褪色,乙烷不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn为正极,Cu为负极,CuCl2溶液作为电解质溶液 | |
| B. | Zn为负极,Cu为正极,稀H2SO4溶液作为电解质溶液 | |
| C. | Zn为负极,Cu为正极,CuSO4溶液作为电解质溶液 | |
| D. | Zn为负极,Fe为正极,Zn发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑥ | B. | ⑤⑦ | C. | ①②⑥ | D. | ③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com