
(1)相同物质的量的O2和O3的质量比________,分子个数比为_______,所含氧原子的个数比为_____。
(2)在20 0 mL 2 mol·L-1MgCl2溶液中,溶质的质量为______。此溶液中
0 mL 2 mol·L-1MgCl2溶液中,溶质的质量为______。此溶液中 Mg2+的物质的量浓度为________,C
Mg2+的物质的量浓度为________,C l-的物质的量浓度为___________________。
l-的物质的量浓度为___________________。
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源:2015-2016学年青海西宁第十四中学高一上期中考试化学卷(解析版) 题型:选择题
下列各种说法中,正确的是( )
A.电离时生成的阳离子全部是氢离子的化合物一定是酸
B.所有的盐电离时只能生成酸根阴离子和金属阳离子。
C.氧化物是指含有氧元素的化合物,如NaOH、H2SO4等。
D.氨气溶于水溶液显碱性,所以氨气属于碱
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西西安第一中学高二上期中考试化学试卷(解析版) 题型:填空题
二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。

(1)硫酸生产中,SO2催化氧化生成SO3 :
:
2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
某温度下,SO2的平衡转化率(a)与体系总压强(p)的关系如右图所示。
根据图示回答下列问题:
①将2.0mol SO2和1.0mol O2置于10L密闭容器中,反应达平衡后,
体系总压强为0.10MPa。该反应的平衡常数等于_______。
②若改在容器中加入1.0 mol SO2、0.5mol O2和amol SO3,保持温度不变反应达 平衡后,体系总压强也为0.10MPa,则a=_________mol。SO2的平衡转化率为_________________。[
平衡后,体系总压强也为0.10MPa,则a=_________mol。SO2的平衡转化率为_________________。[
③平衡状态由A变到B时.平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+C02(g) +2H20(g) △H=-574 kJ·mol-1
+2H20(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H20(g) △H=-1160 kJ·mol-1
若用标准状况下4.48L CH 4还原NO2至N2整个过程中,放出的热量为______kJ。
4还原NO2至N2整个过程中,放出的热量为______kJ。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北武汉华中师大一附中高一上期中化学卷(解析版) 题型:推断题
下图是中学化学中常见物质间的转化关系。其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物;B和E为能产生温室效应的气体且1 mol E中含有 10 mol电子。乙和丁为黑色固体,将它们混和加热后发现固体由黑色变为红色。

(1)写出化学式:甲_________ ;乙________;丙_______;
(2)丁的摩尔质量为 。
(3)写出丙和E反应生成A和B的化学方程式: 。
(4)有学生将乙和丁混和加热后收集到标准状况下气体8.96 L ,测得该气体对氢气的相对密度为16,若将气体通入足量的澄清石灰水中,得到白色沉淀物 g。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北武汉第二中学高二上期中考试化学试卷(解析版) 题型:推断题
下表是不同温度下水的离子积常数:
温度/℃ | 25 | T2 |
水的离子积常数 | 1×10-14 | 1×10-12 |
试回答以下问题:
(1)T2℃时,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=__________。此溶液中各种离子的浓度由大到小的顺序是________________ ____。
(2)25℃时,用0.01mol/LNaOH溶液滴定0.02mol/L 的硫酸,中和后加蒸馏水稀释到5mL,若滴定时终点判断有误差;①多加了1滴NaOH溶液②少加1滴NaOH溶液(设1滴为0.05mL),则①和②溶液中c(OH-)之比是 。
(3)25℃时,0.1mol/L的NaHCO3溶液的pH为8,同浓度的NaAlO2溶液的pH为11。将两种溶液等体积混合,可能发生的现象____________________________________,其主要原因是(用离子方程式表示) 。
(4)已知25℃时:
难溶物 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 |
Ksp | 8.0×10-16 | 8.0×10-38 | 1.0×10-17 |
用废电池的锌皮制备ZnSO4·7H2O的过程中,需去除少量杂质铁,其方法是:加稀硫酸和H2O2溶解。当加碱调节pH为 时,铁刚好完全沉淀而锌开始沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全;假定Zn2+浓度为0.1mol/L)。若上述过程不加H2O2后果和原因是 。(lg2=0.3 lg3=0.48)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北衡水冀州中学高一上月考三文化学卷(解析版) 题型:推断题
实验室用NaOH固体配制250mL 1.25mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制250mL 1.25mol/L的NaOH溶液应称取NaOH的质量是 克。
除量筒、烧杯、玻璃棒、胶头滴管外还需要的其它仪器是 。
(2)容量瓶上需标有以下五项中的 ;
① 温度 ② 浓度 ③ 容量 ④ 压强 ⑤ 刻度线
(3)下列配制的溶液浓度偏低的是 ;
A、定容时俯视刻度线
B、向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
C、加蒸馏水时不慎超过了刻度线
D、配制前,容量瓶中有少量蒸馏水
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北衡水冀州中学高一上月考三理化学卷(解析版) 题型:选择题
下列条件下,两瓶气体所含原子数一定相等的是 ( )
A.同质量、不同密度的N2和CO B.同温度、同体积的H2和N2
C.同体积、同密度的C2H4和C3H8 D.同压强、同体积的N2O和CO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:选择题
对某一可逆反应来说,使用催化剂的作用是
A.提高反应物的平衡转化率
B.改变平衡混合物中某组分的百分含量
C.增大正反应速率,减小逆反应速率
D.以同样程度改变正逆反应的速率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省南昌市高二上学期期中测试化学试卷(解析版) 题型:选择题
对于可逆反应:mA(g)+nB(g)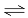 xC(g)+ yD(s) ΔH=?,在不同温度及压强(P1,P2)条件下,反应物A的转化率如下图所示,下列判断正确的是
xC(g)+ yD(s) ΔH=?,在不同温度及压强(P1,P2)条件下,反应物A的转化率如下图所示,下列判断正确的是

A.ΔH>0, m+n>x+y B.ΔH<0, m+n>x+y
C.ΔH<0, m+n>x D.ΔH>0, m+n<x
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com