
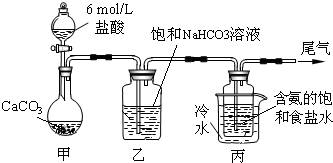
���� ��1��װ�ü����Ʊ�������̼�������к����Ȼ�������Ժ���ʵ��������ţ���Ҫ��ȥ��
��2�����ݷ��������Һ����õ�ʵ������������NaHCO3ת��ΪNa2CO3�ķ����ǹ�����ȷֽ⣻
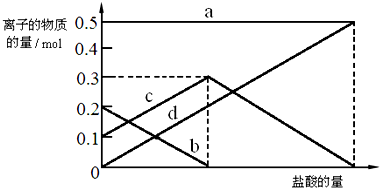
��3���������̼���ƺ�̼�����ƣ��������ᷢ����ӦCO32-+H+=HCO3-�� HCO3-+H+=CO2��+H2O������ͼ�����̼������Ӽ�С��̼������������ࣻ
��4������CO2��NaOH�ķ�Ӧ���ò���Ŀ����������ۣ�
��� �⣺��1��װ�ü����Ʊ�������̼����ķ�Ӧװ�ã����ɵĶ�����̼�����к����Ȼ������壬���Ʊ�̼��������Ӱ�죬װ���ҵ������������Ȼ������壬
�ʴ�Ϊ����ȥCO2�е�HCl��
��2�������NaHCO3����IJ����Ƿ��������Һ�壬�����õ�ʵ������ǹ��˲�����̼���������ȷֽ����ɶ�����̼��̼���ơ�ˮ����ӦΪ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
�ʴ�Ϊ�����ˣ�2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
��3�����ڣ�2�������յ�ʱ��϶̣�NaHCO3���ֽⲻ��ȫ����С���һ�ݼ�����t1min��NaHCO3��Ʒ����ɽ������о���ȡ������t1min��NaHCO3��Ʒ29.6g ��ȫ����ˮ�Ƴ���Һ��Ȼ�������Һ�л����صμ�ϡ���ᣬ�����Ͻ��裮��������ļ��룬������Ӧ CO32-+H+=HCO3-�� HCO3-+H+=CO2��+H2O����Һ���й����ӵ����ʵ����ı仯Ϊ̼������Ӽ�С��̼���������Ũ������̼�������ȫ��ת��Ϊ̼��������ӣ��ٵ��������̼��������ӷ�Ӧ���ɶ�����̼��̼��������Ӽ�С������c���߱�ʾ����̼���������Ũ�ȱ仯��̼�������Ũ��0.2mol/L��̼���������Ũ��Ϊ0.1mol/L����Ʒ��NaHCO3��Na2CO3���ʵ���֮����1��2��
�ʴ�Ϊ��HCO3-��1��2��
��4��CO21.12L����״���£���Ϊ0.05mol��CO2��NaOH��Һ��Ӧʱ������NaOH�Ƿ��������������ۣ�
��NaOH������ǡ����ȫ��Ӧ��0.05molCO2��NaOH��Ӧ������0.05molNa2CO3����Na2CO3������m=nM=0.05mol��106g/mol=5.3g��5.08g���ʼ��費������˵��NaOH���ܹ����������õĹ�����ΪNa2CO3��NaHCO3�����ߵĻ���
�����õĹ�����Na2CO3�����ʵ���ΪXmol��NaHCO3�����ʵ���ΪYmol��
����̼Ԫ�ص��غ���У�X+Y=0.05mol��
�������ù��������Ϊ5.08g���У�106X+84Y=5.08g��
���X=0.04mol Y=0.01mol
�����õĹ����мȺ�Na2CO3�ֺ�NaHCO3��
�������ù�����Na2CO3Ϊ0.04mol��NaHCO3Ϊ0.01mol��������Ԫ�ص��غ��֪��NaOH�����ʵ���n=0.04mol��2+0.01mol=0.09mol��
��NaOH�����ʵ���Ũ��C=$\frac{n}{V}$=$\frac{0.09mol}{0.1L}$=0.9mol/L��
�ʴ�Ϊ��Na2CO3��NaHCO3�� 0.9 mol/L��
���� ���⿼���� ��ҵ�ƴ����ԭ�����������������е����ʱ仯�������ɷֵķ����жϺͼ���Ӧ�ã�ʵ����̷��������Ӳ�����β�����գ�ͼ���������жϣ���Ŀ�Ѷ��еȣ�


 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д� �߽�������ϵ�д�
�߽�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 150mL1mol•L-1��NaCl��Һ | B�� | 75mL4mol•L-1��NH4Cl��Һ | ||
| C�� | 75mL1mol•L-1��FeCl3��Һ | D�� | 150mL2mol•L-1��KCl��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
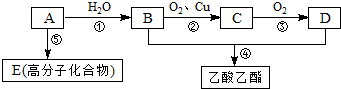
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼������ | B�� | �������� | C�� | �ʰ��� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��һ�ֿ�����ҩ�������ͼ��ʾ��ת����ϵ��
��һ�ֿ�����ҩ�������ͼ��ʾ��ת����ϵ��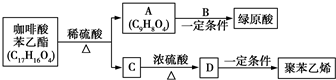
 ��
��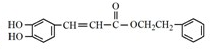 ��
�� ����д1������
����д1�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2CO3��NaHCO3�����ε���Һ�У����������ͬ | |
| B�� | ������1mol/L��CH3COOH��Һ��1mol/L��NaOH��Һ�������ϣ����û��Һ��c ��CH3COO-����c��Na+����c��OH-����c��H+�� | |
| C�� | ���ʵ����ʵ���Ũ����ͬ��NH4Cl��NH4HSO4������Һ�У�c��NH4+��ǰ��С�ں��� | |
| D�� | �����£�ij��Һ����ˮ�������c��H+��Ϊ10-5mol/L�������Һ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
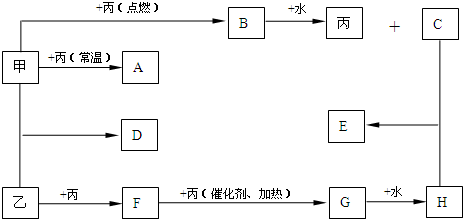
 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com