
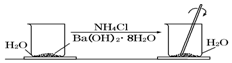
 在研究化学反应中的能量变化时,我们通常做下面的实验:
在研究化学反应中的能量变化时,我们通常做下面的实验:分析 (1)反应为复分解反应,二者反应生成氨气、水、以及氯化钡;
(2)玻璃棒的搅拌作用是使混合物混合均,让化学反应快速发生;
(3)根据反应是否充分进行分析;
(4)水排开了烧杯底部与玻璃片之间的空气,压强的作用使烧杯与玻璃片“黏在一起.
解答 解:(1)氯化铵属于铵盐,能和强碱氢氧化钡反应生成氨气、水、以及氯化钡,化学方程式为Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O,
故答案为:Ba(OH)2•8H2O+2NH4Cl═BaCl2+10H2O+2NH3↑;
(2)Ba(OH)2•8H2O晶体和氯化铵晶体之间的反应是固体之间的反应,搅拌可使混合物充分接触并发生反应,
故答案为:使反应物充分混合,迅速发生反应,使体系的温度降低;
(3)①反应物未进行快速搅拌;②玻璃片上滴加的水太多;③氢氧化钡晶体已部分失水;④环境温度太高;⑤试剂用量太少;⑥氢氧化钡晶体未研成粉末,可能看不到“结冰”现象,
故答案为:①反应物未进行快速搅拌;②玻璃片上滴加的水太多;③氢氧化钡晶体已部分失水;④环境温度太高;⑤试剂用量太少;⑥氢氧化钡晶体未研成粉末;
(4)水排开了烧杯底部与玻璃片之间的空气,外压大于内压,烧杯与玻璃片黏在一起了,
故答案为:水排开了烧杯底部与玻璃片之间的空气,在大气压的作用下,烧杯与玻璃片黏在一起了.
点评 本题考查了化学反应中的能量变化,以Ba(OH)2•8H2O与NH4Cl固体的反应为背景考查了分析问题、解决问题的能力和实验设计能力,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 合金的性能一般优于纯金属 | |
| B. | 碳素钢是目前用量最大的合金,碳素钢在空气中比纯铁耐腐蚀 | |
| C. | 酒精灯加热铝箔至熔化,铝并不滴落,说明铝表面生成一层致密的氧化膜 | |
| D. | 用金属铝与V2O5反应冶炼钒,主要是因为铝的还原能力比钒强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯、环己烯 | B. | 乙酸和甲酸甲酯 | ||
| C. | 对甲苯酚和苯甲醇 | D. | 甲醛和甲酸甲酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与稀盐酸反应:Fe+2H+═Fe2++H2↑ | |
| B. | 氢氧化钠溶液与盐酸反应:OH-+H+═H2O | |
| C. | 铝与硫酸铜溶液反应:Al+Cu2+═Al3++Cu | |
| D. | 氯化钡溶液与稀硫酸反应:SO42-+Ba2+═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用CO2合成聚碳酸酯可降解塑料,可实现“碳”的循环利用 | |
| B. | 油脂都不能使溴的四氯化碳溶液褪色 | |
| C. | 液化石油气和天然气的主要成分都是烃 | |
| D. | 煤是由有机物和少量无机物组成的复杂混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
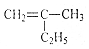
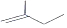
 的名称2,3,5-三甲基-4-乙基庚烷
的名称2,3,5-三甲基-4-乙基庚烷 ,
,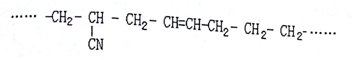
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式: | B. | N2的结构式:N≡N | C. | H2O的球棍模型: | D. | CH4的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
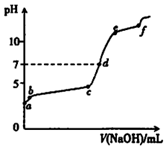 向0.1mol/L的Al2( SO4)3溶液中滴加1.0mol/L的NaOH溶液,滴加过程中溶液pH随NaOH溶液体积变化的曲线如图所示.下列分析不正确的是( )
向0.1mol/L的Al2( SO4)3溶液中滴加1.0mol/L的NaOH溶液,滴加过程中溶液pH随NaOH溶液体积变化的曲线如图所示.下列分析不正确的是( )| A. | a点pH<7的原因:Al3++3H2O?Al(OH)3+3H+ | |
| B. | bc段发生的主要反应:Al3++3OH-═Al(OH)3 | |
| C. | ef段发生的主要反应:Al(OH)3+OH-═AlO2-+2H2O | |
| D. | d点,溶液中大量存在的离子是Na+、AlO2-和SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com