
【题目】化学兴趣小组向同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
实验Ⅰ:制取NaClO2晶体
已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。现利用下图所示装置进行实验。
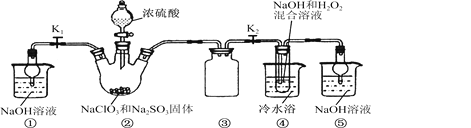
(1)装置③的作用是____________________。
(2)装置②中产生ClO2的化学方程式为________________ ;装置④中制备NaClO2的化学方程式为____________________。
实验Ⅱ:测定某亚氯酸钠样品的纯度。
设计如下实验方案,并进行实验:
①准确称取所得亚氯酸钠样品mg于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO2-+4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250 mL待测溶液。②移取25.00 mL待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得平均值为V mL(已知:I2+2S2O32-=2I-+S4O62-)。
(3)该样品中NaClO2的质量分数为____________(用含m、c、V的代数式表示)。
(4)在滴定操作正确无误的情况下,此实验测得结果偏高,原因用离子方程式表示为______________。
【答案】 防止倒吸 2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O 2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2 ![]() % 4I-+O2+4H+=2I2+2H2O
% 4I-+O2+4H+=2I2+2H2O
【解析】本题主要考查物质的制备和测量物质的含量。(1)根据反应装置图可知:装置④中气体反应,装置内压强降低,装置③防止倒吸;(2)装置②中氯酸钠被还原为ClO2,则亚硫酸钠被氧化为硫酸钠,其反应的化学方程式为:2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O;装置④反应后的溶液获得NaClO2晶体,故装置④中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,根据升降法配平后方程式为:2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;
(3)根据方程式可得关系式为:NaClO2~2I2~4S2O32-,该样品中NaClO2的质量分数为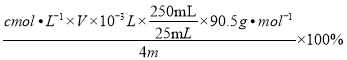 =
=![]() %;(4)实验测得结果偏高,说明滴定消耗的Na2S2O3标准液体积偏高,溶液中碘的含量偏高,应是生成的碘离子被氧气氧化为碘,同时生成水,反应离子方程式为4I-+O2+4H+=2I2+2H2O。
%;(4)实验测得结果偏高,说明滴定消耗的Na2S2O3标准液体积偏高,溶液中碘的含量偏高,应是生成的碘离子被氧气氧化为碘,同时生成水,反应离子方程式为4I-+O2+4H+=2I2+2H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】1.52g铜镁合金完全溶解于50mL密度为1.40g·mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0 mol·L-1NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )
A. 该合金中铜与镁的物质的量之比是2:1
B. 该浓硝酸中HNO3的物质的量浓度是14.0 mol·L-1
C. NO2和N2O4的混合气体中,NO2的体积分数是60%
D. 得到2.54 g沉淀时,加入NaOH溶液的体积是640 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列关于H2S和SO2的说法正确的是______________
A.两气体都可用浓硫酸干燥
B.两气体均可以用NaOH溶液吸收
C.两气体按体积比1:2 混合可完全转化为S
D.将两气体通入溴水或酸性KMnO4溶液中,可通过颜色变化鉴别两气体
(2)目前治理汽车尾气是在催化剂条件下发生反应2NO+2CO![]() N2+2CO2,现在实验室模拟上述反应,己知在t℃时在2L恒容密闭容器中加入2 molNO和1mol CO气体,经l0min达到平衡,测得此时CO2的体积分数为1/7,回答下列问题:
N2+2CO2,现在实验室模拟上述反应,己知在t℃时在2L恒容密闭容器中加入2 molNO和1mol CO气体,经l0min达到平衡,测得此时CO2的体积分数为1/7,回答下列问题:
①这段时间内CO的反应速率为_________________ 。
②该反应平衡常数______________(保留两位有效数字)。
③平衡后再向密闭容器通入0.4molCO和0.4molCO2,平衡将_____________(填“正向”、“逆向”或“不”)移动。判断理由是_________________。
④若升温发现体系气体平均相对分子质量增大,则该反应的△H______0(填“>”、“<”或“=”)。
⑤维持条件不变,向平衡后的容器再充入0.2molNO和0.1molCO,达到新平衡,则与原平衡相比NO的转化率____________ (填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,某NaOH稀溶液中c(H+)=10a mol/L,c(OH)=10b mol/L,已知a+b=12,请回答下列问题:
(1)该温度下水的离子积常数KW=__________________。
(2)NaOH的物质的量浓度为_________________,由水电离出的c(OH)为______________。
(3)给该NaOH溶液降温,pH________(填“变大”、“变小”或“不变”)。
(4)该温度下,将pH=3的H2SO4与pH=11的NaOH等体积混合,则混合后溶液的pH=____(已知lg2=0.3) (忽略溶液体积变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液一定是碱性的是 ( )
A. 溶液中c(OH-)>c(H+) B. c(OH-)>1×10-7mol/L
C. 溶液中含有OH- D. pH=8的某电解质的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车发动机在工作时,由于电喷,在气缸中会发生反应:N2(g)+O2 (g)=2NO(g).已知该反应过程中的能量变化如图所示,下列说法中不正确的是( ) 
A.该反应是放热反应
B.该反应是氧化还原反应
C.该反应过程中有共价键的断裂和形成
D.使用催化剂可以改变反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com