
| 选项 | 实验 | 现象 | 结论 |
| A | 将等物质的量的SO2与Cl2混合后,通入品红溶液 | 品红褪色 | SO2、Cl2都能使品红褪色 |
| B | 将Fe2O3溶于足量氢碘酸溶液,然后滴入淀粉溶液 | 溶液变蓝 | 氧化性:Fe3+>I2 |
| C | 注射器中吸入NO2,封堵针尖处,将注射器体积压缩为原来的一半 | 气体颜色比起始时浅 | 加压后,NO2转变为无色的N2O4 |
| D | 饱和BaSO4悬浊液中加入饱和Na2CO3溶液,振荡,然后过滤、洗涤,向所得固体中加入盐酸 | 沉淀部分溶解且有气体产生 | Ksp(BaSO4)> Ksp(BaCO3) |
| A. | A | B. | B | C. | C | D. | D |
分析 A.将等物质的量的SO2与Cl2混合,发生反应生成盐酸和硫酸;
B.溶液变蓝,说明生成碘单质;
C.增大压强,浓度增大,颜色加深;
D.如满足Qc>Ksp,可生成沉淀.
解答 解:A.将等物质的量的SO2与Cl2混合,发生反应生成盐酸和硫酸,品红不褪色,现象不正确,故A错误;
B.溶液变蓝,说明生成碘单质,可说明氧化性:Fe3+>I2,故B正确;
C.增大压强,浓度增大,虽然平衡正向移动,但颜色加深,故C错误;
D.BaSO4饱和溶液中加入饱和Na2CO3溶液有白色沉淀,是因为碳酸根离子浓度大,和钡离子浓度乘积等于碳酸钡的Ksp,实际Ksp(BaSO4)小于Ksp(BaCO3),故D错误.
故选B.
点评 本题考查较为综合,涉及物质的性质、检验、平衡移动以及难溶电解质的溶解平衡等知识,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的严密性和可行性的评价,难度不大.


 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:选择题
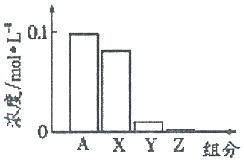 常温下,0.2moI•L-l的Na2CO3溶液与0.2moI•L-l的盐酸等体积混合后,所得溶液中部分微粒组分与浓度的关系如图所示,X、Y、Z均表示含碳微粒,下列说法正确的是( )
常温下,0.2moI•L-l的Na2CO3溶液与0.2moI•L-l的盐酸等体积混合后,所得溶液中部分微粒组分与浓度的关系如图所示,X、Y、Z均表示含碳微粒,下列说法正确的是( )| A. | A代表Na+浓度 | |
| B. | 该溶液中c(OH-)>c(Y) | |
| C. | 向该溶液中加水稀释,所有离子浓度均减小 | |
| D. | 该混合溶液中:c(X)+c(Y)+c(Z)═2c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
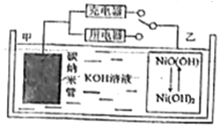 氢燃料电池具有广阔前景.某二次氢燃料电池的原理如图所示,该电池用吸附了H2的碳纳米管等材料制作而成,下列说法正确的是( )
氢燃料电池具有广阔前景.某二次氢燃料电池的原理如图所示,该电池用吸附了H2的碳纳米管等材料制作而成,下列说法正确的是( )| A. | 放电时,甲电极为正极,OH-移向乙电极 | |
| B. | 可开发氢燃料电池用于电动汽车 | |
| C. | 电池总反应为H2+NiO(OH)$?_{充电}^{放电}$Ni(OH)2 | |
| D. | 充电时,乙电极反应式为NiO(OH)+H2O+e-=Ni(OH)2+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗铜作阳极 | |
| B. | 用CuSO4溶液作电解液 | |
| C. | 阴极的电极反应式:Cu2++2e-=Cu | |
| D. | 当阳极质量减少ag时,阴极质量增加ag |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在电解精炼铜时,当电路中通过的电子数为2NA时,阳极质量减少64g | |
| B. | 标准状况下,22.4 LCO和C2H4混合气体的总分子数为NA,质量为28g | |
| C. | 常温常压下,1mol甲基(-CH3)所含电子数为10NA | |
| D. | 标准状况下,11.2L苯中含有C-H键的数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,向含Ag2S固体的溶液中滴加少量Na2S溶液,c(Ag+)、c(S2-)、Ksp(Ag2S)都减小 | |
| B. | 常温下,pH=10的K2CO3溶液和pH=4的FeCl3溶液中,水的电离程度后者小 | |
| C. | 含KHSO3和K2SO3的中性混合溶液中有c(K+)=c(HSO3-)+2c(SO32-) | |
| D. | 常温下,将pH=2的HX溶液稀释1000倍,稀释后溶液的pH一定为5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 短周期主族元素,a、b、c、d的原子序数依次增大.四种元素形成的单质依次为m、n、p、q,其 中q为淡黄色固体;x、y、z是这些元素组成的二元化合物;25℃,0.01mol•L-1w溶液中$\frac{c({H}^{+})}{c(O{H}^{-})}$=1.0×10-10.上述物质的转化关系如图所示.下列说法正确的是 ( )
短周期主族元素,a、b、c、d的原子序数依次增大.四种元素形成的单质依次为m、n、p、q,其 中q为淡黄色固体;x、y、z是这些元素组成的二元化合物;25℃,0.01mol•L-1w溶液中$\frac{c({H}^{+})}{c(O{H}^{-})}$=1.0×10-10.上述物质的转化关系如图所示.下列说法正确的是 ( )| A. | 离子半径的大小:a<b<c<d | |
| B. | b氢化物的沸点高于主族其它元素氢化物的沸点 | |
| C. | 将b、c、d组成的化合物加入到水中对水的电离没有影响 | |
| D. | y、w含有的化学键类型完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
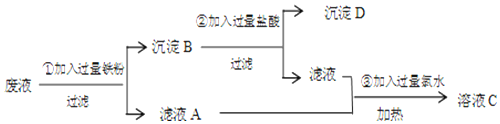
| A. | 加入过量氨水:NH4+、Cl-、[Cu(NH3)4]2+ | |
| B. | 通入过量Cl2:Fe2+、Cu2+、C-、H+ | |
| C. | 加入过量铁粉:Cu2+、Fe2+、Cl-、H+ | |
| D. | 加入过量KSCN溶液:Na+、K+、Fe3+、H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com