
| A�� | �٢ۢܢ� | B�� | �ۢܢ� | C�� | �٢ڢ� | D�� | ȫ�� |
���� ��ǿ��������ʹ�����ʷ������ԣ�
�ڱ�����ʹ�����ʷ������ԣ��������ж���
���Ʊ��ᣬ�Ҵ�������Ϊ���
����ά��Ϊ���ǣ��������к�-CONH-��
�ݼ������С�մ�ϡ��ˮ������Ӧ���������ԣ���С�մ�ϡ��ˮ���Խ�����
��� �⣺��ǿ��������ʹ�����ʷ������ԣ����˵�Ƥ����ǿ�����ߵ������½���ʧȥ�������ԣ�����ȷ��
�ڱ�����ʹ�����ʷ������ԣ��������ж����������ñ��Ӷ�ʳ���������ʴ���
���Ʊ��ᣬ�Ҵ�������Ϊ���ᣬ������������Ӧ������ȷ��
����ά��Ϊ���ǣ���������˿����Ҫ�ɷֶ�����ά�أ��������к�-CONH-����˿��֩��˿����Ҫ�ɷֶ��ǵ����ʣ�����ȷ��
�ݼ������С�մ�ϡ��ˮ������Ӧ���������ԣ���С�մ�ϡ��ˮ���Խ���������϶�ҧ�˵�Ƥ��ʱ�����������ע�����壬���ڻ���ͿĨС�մ��ϡ��ˮ������ȷ��
��ѡA��
���� ���⿼���л���Ľṹ�����ʣ�Ϊ��Ƶ���㣬���չ����������ʵĹ�ϵ���л������ɡ��л���ӦΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע�⻯ѧ���������ϵ����Ŀ�ѶȲ���


 ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ���� | B�� | �������� | C�� | Ũ���� | D�� | ����ͭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2��SO3 | B�� | HCl��NaCl | C�� | KI��I2 | D�� | Fe2O3��Fe |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1 | B�� | 1��2 | C�� | 1��3 | D�� | 3��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��С���ʹѹǿ���� | B�� | �����¶� | ||
| C�� | ����������H2ʹѹǿ���� | D�� | ѹǿ�������ϡ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ��������b��a��c��d | B�� | ԭ�Ӱ뾶��C��D��A��B | ||
| C�� | ���Ӱ뾶��Cn-��D��n+1��-��An+��B��n+1��+ | D�� | ���ʻ�ԭ�ԣ�A��B��C��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
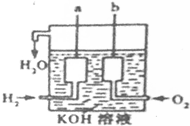 ��1����������������ɴ���ʹ����һ������װ�ã��乹����ͼ��ʾ��a��b�����缫���ɶ��̼����ɣ�д��b���ĵ缫��Ӧ����ʽ������ʱ��ظ�������pH��С�����������С�����䡱����
��1����������������ɴ���ʹ����һ������װ�ã��乹����ͼ��ʾ��a��b�����缫���ɶ��̼����ɣ�д��b���ĵ缫��Ӧ����ʽ������ʱ��ظ�������pH��С�����������С�����䡱�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���ữѧʽ | HClO | H2CO3 |
| ����ƽ�ⳣ�� | K=4.7��10-8 | K1=4.3��10-7��K2=5.6��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
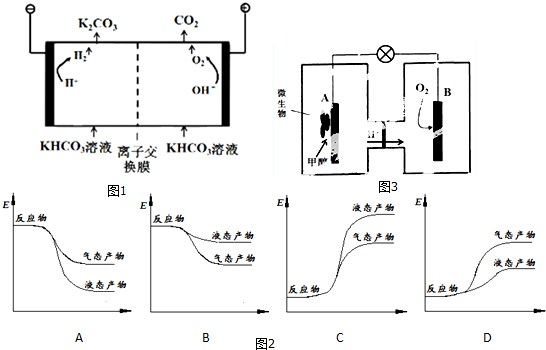
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com