
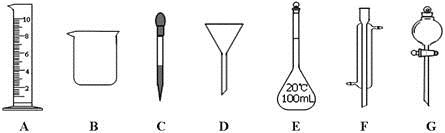
(1)д���������ƣ� F ��
(2)����ʵ��������õ�����G���� (ѡ������ѡ��ı����ĸ)��
a������ˮ��CC14�Ļ���� b������ˮ�;ƾ��Ļ���� c������ˮ����ɰ�Ļ����
(3)ʵ��������210mL 0.5mol/L��������Һ��
�����й�������E��ʹ�÷����У���ȷ���� (ѡ������ѡ��ı����ĸ)��
a��ʹ��ǰӦ����Ƿ�©Һ b��ʹ��ǰ������
c�������������ʷ�Ӧ���ܽ������ d������Һ��ֱ��ת�Ƶ�����ƿ��
������ȡ10mol/L��Ũ���� mL��ȡ�ø��������ʱ����Ҫ�õ����������е�A�� (ѡ�������ı����ĸ)��
 �߲������Ӧ��һ��ͨϵ�д�
�߲������Ӧ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017��ӱ�ʡ�����ϵ����Ļ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����
A����FeCl3��Һ��Ͷ��������Zn�ۣ�2Fe3++ Zn==Zn2++ 2Fe2+
B������������(Fe3O4)��������Fe3O4 + 8H+=Fe2+ + 2Fe3++4H2O
C��NaHSO4��Һ��Ba(OH)2��Һ��Ϻ�����ԣ� 2H++ SO42-+Ba2++ 2OH- =BaSO4��+2H2O
D��Ca(ClO)2��Һ��ͨ������SO2��Ca2++ 2ClO-+SO2+ H2O=CaSO3��+ 2HC1O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ĸ������¿��Ļ�ѧ���������棩 ���ͣ�ѡ����
��ͼ��ʾ������˵����ȷ����( )
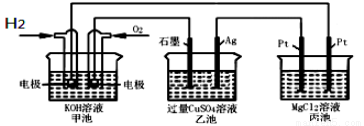
A���׳�ͨ��O2�ĵ缫��ӦΪO2 + 4e-+ 4H+��2H2O
B���ҳ� Ag�缫����6.4g����Һ�н�ת��0.2mol����
C����Ӧһ��ʱ������ҳ��м���һ����Cu(OH)2���壬��ʹCuSO4��Һ�ָ���ԭŨ��
D���׳�������280 mL(��״����)O2����ʱ������������������1.45g����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ����12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ͼ1Ϊ�����O2���ɵ�ȼ�ϵ��ʾ��ͼ�������ΪKOH��Һ��ͼ2Ϊ���AlCl3��Һ��װ�ã��缫���Ͼ�Ϊʯī���ø�װ�ý���ʵ�飬��Ӧ��ʼ��۲쵽x�缫�������ְ�ɫ����������˵����ȷ����
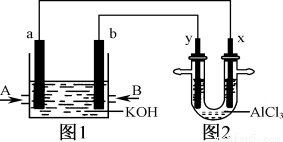
A��ͼ1�е������Һ��pH����
B��ͼ2�е��AlCl3��Һ���ܷ�ӦΪ2Cl����2H2O Cl2����H2����2OH��
Cl2����H2����2OH��
C��A��ͨ�������ΪCH4���缫��ӦʽΪCH4��10OH����8e��= CO32����7H2O
D��������Cl����x���ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ����12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йػ�ѧ����ı�ʾ��ȷ����
A��HBrO�ĵ���ʽ��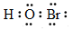
B����Ȳ�ķ��ӽṹģ��ʾ��ͼ��
C��������Ϊ18����ԭ�ӽṹʾ��ͼ��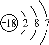
D��̼�����Ƶĵ��뷽��ʽ��NaHCO3 Na����H����CO
Na����H����CO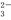
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ��һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪�з�Ӧ��3Fe2++2S2O32��+O2+xOH��==Fe3O4+S4O62��+2H2O���� ��˵���в���ȷ����
��˵���в���ȷ����
A��x=4
B��Fe2+��S2O32�����ǻ�ԭ��
C��1molFe2+������ʱ����Fe2+��ԭ��O2�����ʵ���Ϊ1/3mol
D��ÿ����1molFe3O4����Ӧת�Ƶ��ܵ��ӵ����ʵ���Ϊ4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ��һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA���������ӵ���������ֵ�������й�������ȷ����
�ٱ�״���£�2.24LH2O���еķ���������0.1NA
��23gNa����������ȫ����ʧ������һ��ΪNA
��1mol����������������������ΪNA
�ܳ��³�ѹ�£�32gO2��O3������������Ϊ16 NA
����CO2��O2��ɵĻ�����й���NA�����ӣ����е���ԭ����Ϊ2 NA
A���٢ڢ� B���ڢۢ� C���ۢܢ� D���ڢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ��һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
������4λͬѧ�ԡ���ѧ�뽡������һ���ⷢ���ļ��⣬������ȷ����
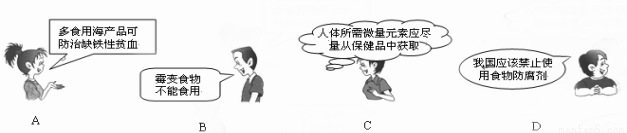
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ɽ��ʡ�߶�12�¼�⻯ѧ�Ծ��������棩 ���ͣ������
��֪25��ʱ����������ʵĵ���ƽ�ⳣ���������±���
��ѧʽ | CH3COOH | H2CO3 | HClO | |
ƽ�ⳣ�� | Ka=1.8��10-5 | Ka1=4.3��10-7 | Ka2=5.6��10-11 | Ka=3.0��10-8 |
�ش��������⣺
(1) ���ʵ���Ũ�Ⱦ�Ϊ0��1mol��Lһ1��������Һ��a��CH3COONa b��Na2CO3 c��NaClO d��NaHCO3��pH��С���������˳����___________ (����ĸ��ʾ)
(2) �����£�0��1mol��L��1��CH3COOH��Һ��ˮϡ�����У����б���ʽ�����ݱ�����_______ (�����)
A��c��H+�� B��c(H+)��c(CH3COOH)
C��c(H+)��c(OH��) D��c(OH-)��c(H+)
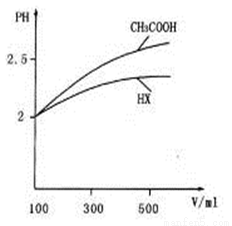
(3) �����Ϊl00mL pH=2��CH3COOH��һԪ��HX����ˮϡ������pH����Һ����Ĺ�ϵ��ͼ��ʾ����HX�ĵ���ƽ�ⳣ��_______ (���������������=��)CH3COOH�ĵ���ƽ�ⳣ����
(4) 25��ʱ����CH3COOH��CH3COONa�Ļ����Һ�У������pH=6������Һ�У�
�� c(CH3COO��)��c(Na+)=_______ mol��L��1(�ȷֵ)
�� c(CH3COO-)��c(CH3COOH)=_______ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com