
【题目】某溶液中存在NH4+、Cl-、H+、OH-四种离子。下列各离子浓度关系一定不正确的是( )
A.c(NH4+)+c(H+)=c(Cl-)+c(OH-)
B.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C.c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.c(NH4+)=c(Cl-)>c(H+)=c(OH-)
【答案】C
【解析】
A.在溶液中,阴阳离子所带的电荷的物质的量相等,有电荷守恒,则c(NH4+)+c(H+)=c(Cl-)+c(OH-),正确,A不符合题意;
B.在NH4Cl溶液中,由于NH4+水解,c(Cl-)>c(NH4+);由于NH4+结合水电离出来的OH-,NH4++H2O![]() NH3·H2O+H+,使得c(H+)>c(OH-),水解是微弱的,c(NH4+)>c(H+),综合排序为c(Cl-)>c(NH4+)>c(H+)>c(OH-),正确,B不符合题意;
NH3·H2O+H+,使得c(H+)>c(OH-),水解是微弱的,c(NH4+)>c(H+),综合排序为c(Cl-)>c(NH4+)>c(H+)>c(OH-),正确,B不符合题意;
C.在溶液中,若c(NH4+)>c(Cl-)>c(H+)>c(OH-),则c(NH4+)+c(H+)>c(Cl-)+c(OH-),溶液不呈电中性,不符合事实,错误,C符合题意;
D.当溶液呈中性的时候,c(H+)=c(OH-),根据电荷守恒,有 c(NH4+)=c(Cl-),正确,D不符合题意。
答案选C。


科目:高中化学 来源: 题型:
【题目】工业制硫酸中的一步重要反应是SO2在400~600 ℃下的催化氧化:2SO2+O2![]() 2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是( )
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是( )
A. 使用催化剂是为了加快反应速率,提高生产效率
B. 在上述条件下,SO2不可能100%地转化为SO3
C. 为了提高SO2的转化率,应适当提高O2的浓度
D. 达到平衡时,SO2的浓度与SO3的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积可变的密闭容器中加入WO3和H2进行反应:WO3(s)+3H2(g)![]() W(s)+3H2O(g),下列说法不正确的是( )
W(s)+3H2O(g),下列说法不正确的是( )
A.将容器的体积缩小一半,其反应速率增大
B.保持体积不变,充入氩气,其反应速率不变
C.保持压强不变,充入氖气,H2O(g)的生成速率增大
D.保持压强不变,充入氖气,H2O(g)、H2(g)的生成速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)锂空气电池比传统的锂离子电池拥有更强的蓄电能力,是传统锂离子电池容量的10倍,其工作原理示意图如图。

放电时,b电极为电源的__极,电极反应式为__。
(2)汽车尾气中CO、NO2在一定条件下可发生反应4CO(g)+2NO2(g)![]() 4CO2(g)+N2(g),一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示。
4CO2(g)+N2(g),一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示。

①0~10min内该反应的平均反应速率v(CO)=__。
②恒温恒容条件下,不能说明该反应已经达到平衡状态的是__(填序号)。
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.容器内混合气体密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二次电池充放电时总反应可表示为Fe+Ni2O3+3H2O![]() Fe(OH)2+2Ni(OH)2,下列说法正确的是( )
Fe(OH)2+2Ni(OH)2,下列说法正确的是( )
A.该电池可用H2SO4溶液作电解液
B.放电时,当有1molFe(OH)2生成时,电解质溶液中通过的电子数为2NA
C.放电时,Fe所在的电极发生还原反应
D.充电时,阳极的电极反应式为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列叙述正确的是( )
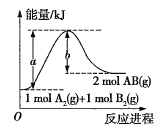
A.该反应是放热反应
B.由图可知,1molA2(g)和1molB2(g)反应生成2molAB(g)放出bkJ热量
C.由图可知,1molA2(g)和1molB2(g)反应生成2molAB(g)吸收bkJ热量
D.由图可知,1molA2(g)和1molB2(g)反应生成2molAB(g)吸收(a-b)kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物(主要为NO和NO2)是大气污染物,如何有效地消除氮氧化物的污染是目前科学家们研究的热点问题。
(1)用尿素[CO(NH2)2]吸收氮氧化物是一种可行的方法。
①尿素在高温条件下与NO2反应转化成无毒气体,该反应的化学方程式为___。用尿素溶液也可吸收氮氧化物,研究表明,当混合气体中![]() =1时,总氮还原率最高,随着,
=1时,总氮还原率最高,随着,![]() 比值增大,总氮还原率降低的主要原因是___。
比值增大,总氮还原率降低的主要原因是___。
②在一个体积为1L的恒容密闭容器中充入1molCO2和1molNH3,在恒定温度下使其发生反应2NH3(g)+CO2(g)![]() NH2CONH2(s)+H2O(g) △H<0并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示。
NH2CONH2(s)+H2O(g) △H<0并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示。

则A点时v正(CO2)___(填“>”“<”或“=”)B点时v正(CO2),原因是___。B点时,NH3的转化率为___。
③下列有关反应2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)的说法正确的是___。
CO(NH2)2(s)+H2O(g)的说法正确的是___。
A.分离出少量的尿素,NH3的转化率将增大
B.反应达到平衡时,降低反应体系的温度,CO2的浓度减小
C.NH3的转化率始终等于CO2的转化率
D.加入有效的催化剂能够提高尿素的产率
(2)已知O3氧化氮氧化物的主要反应的热化学方程式如下:
2NO(g)+O2(g)=2NO2(g) △H1=akJ·mol-1
NO(g)+O3(g)=NO2(g)+O2(g) △H2=bkJ·mol-1
6NO2(g)+O3(g)=3N2O5(g) △H3=ckJ·mol-1
则反应4NO2(g)+O2(g)=2N2O5(g)△H=___(用含a、b、c的代数式表示)kJ·mol-1。
(3)氮氧化物也可用碱液吸收。若NO和NO2的混合气体被NaOH溶液完全吸收,只生成一种盐,则该盐的化学式为___;已知常温下Ka(HNO2)=5×10-4,则反应HNO2(aq)+NaOH(aq)![]() NaNO2(aq)+H2O(l)的平衡常数K=___。
NaNO2(aq)+H2O(l)的平衡常数K=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中CO、![]() 在一定条件下可发生反应
在一定条件下可发生反应![]() ,一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和
,一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和![]() ,
,![]() 的物质的量随时间的变化曲线如图所示:
的物质的量随时间的变化曲线如图所示:

(1)0~10min内该反应的平均反应速率![]() ________
________
(2)恒温恒容条件下,不能说明该反应已经达到平衡状态的是________(填序号)
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.容器内混合气体密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计的二氧化碳的熔盐捕获及电化学转化装置如图所示。下列说法正确的是( )
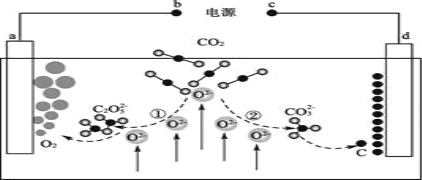
A.a极是电化学装置的阴极
B.d极的电极反应式为CO32- - 4e- = C + 3O2-
C.①中,捕获CO2时碳元素的化合价发生了变化
D.上述装置中反应的化学方程式为CO2 ![]() C + O2↑
C + O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com