
| 3 |
| ||
| 10-14 |
| 10-9 |


 ����ѧ����ϵ�д�
����ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ����� | ƽ�ⷽ��ʽ | ƽ�ⳣ��K | Ksp |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76��10-5 | |
| H2CO3 | H2CO3???H++HCO3- HCO3-???H++CO32- | K1=4.31��10-4 K2=5.61��10-11 | |
| C6H5OH | C6H5OH???C6H5O-+H+ | 1.1��10-10 | |
| H3PO4 | H3PO4???H++H2PO4- H2PO4-???H++HPO42- HPO42-???H++PO43- | K1=7.52��10-3 K2=6.23��10-8 K3=2.20��10-13 | |
| NH3?H2O | NH3?H2O???NH4++OH- | 1.76��10-5 | |
| BaSO4 | BaSO4??Ba2++SO42- | 1.07��10-10 | |
| BaCO3 | BaCO3???Ba2++CO32- | 2.58��10-9 |
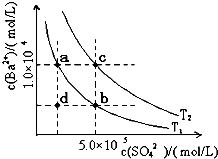 �ش��������⣺
�ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��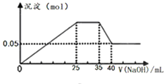 ��ʾ��Mg2+��Al3+��NH4+������Һ�еμ�NaOH��Һʱ������������NaOH������Ĺ�ϵͼ�����������ӵ����ʵ���֮��Ϊ��n��Mg2+����n��Al3+����n�� NH4+��=2��1��2������ʹ�õ�NaOH��Ũ��Ϊ2mol?L-1�� |
B��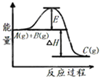 �����߱�ʾij��Ӧ���̵������仯��������A��g����B��g����Ӧ��������C��g��ʱ����H��0����ʹ����������Eֵ���С�� |
C��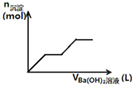 ��������ʾ�������ữ��MgSO4��Һ�м���Ba��OH��2��Һʱ���������������ʵ�����n�������Ba��OH��2��Һ�����V��֮��Ĺ�ϵͼ |
D��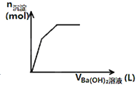 ��ʾ��һ��������������Һ�еμ�Ba��OH��2��Һʱ���������������ʵ�����n�������Ba��OH��2��Һ�����V��֮��Ĺ�ϵͼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | Cu��OH��2 | Fe��OH��3 | CuCl | CuI |
| Ksp | 2.2��10-20 | 2.6��10-39 | 1.7��10-7 | 1.3��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
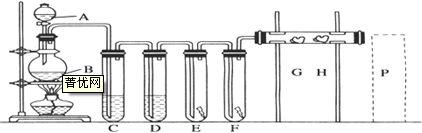
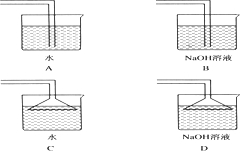
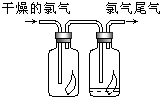 ��1����ͼ��ʾ������������ͨ��ʢ�и�����ɫ�����Ĺ��ƿ��ʢ�г�ʪ��ɫ�����Ĺ��ƿ���ɹ۲쵽��������
��1����ͼ��ʾ������������ͨ��ʢ�и�����ɫ�����Ĺ��ƿ��ʢ�г�ʪ��ɫ�����Ĺ��ƿ���ɹ۲쵽���������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��AlCl3 |
| B��KHCO3 |
| C��Fe2��SO4��3 |
| D��NH4HCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ڿ�����ȼ�ղ�����ɫ���棬���ɵ���ɫ�������� |
| B��������ˮ��dz����ɫ����ˮ���������pH����� |
| C������ϡ���ᷴӦ�����Ȼ�������������������Ӧ���������Ȼ��� |
| D��Ư�۵���Ч�ɷ��Ǵ�����ƣ�������Ư��������Ϊ��ˮ��Һ����������ǿ�����ԵĴ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com