
氮化钠和氢化钠分别与水反应的化学方程式如下:Na3N + 3H2O=3NaOH + NH3↑,
NaH + H2O=NaOH + H2↑。有关Na3N和NaH的叙述正确的是( )
A.离子半径:Na+>N3->H+
B.加热熔化时,都只破坏离子键
C.与盐酸反应都只生成一种盐
D.上述反应都是氧化还原反应
科目:高中化学 来源:2016-2017学年河北省高二上9月调研化学试卷(解析版) 题型:选择题
某烃有两种或两种以上的同分异构体,其同分异构体中的某一种的一氯代物只有一种,则这种烃可能是
①分子中具有7个碳原子的芳香烃;
②分子中具有4个碳原子的烷烃;
③分子中具有12个氢原子的烷烃;
④分子中具有8个碳原子的烷烃。
A.③④ B.①② C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上开学测化学试卷(解析版) 题型:实验题
铁、铜等金属及其化合物在日常生产生活中用途非常广泛.
Ⅰ.实验室欲制备0.3mol Cu(NO3)2晶体,甲、乙两同学分别设计实验方案如下:
甲:Cu Cu(NO3)2 ;乙:Cu
Cu(NO3)2 ;乙:Cu CuO
CuO  Cu(NO3)2
Cu(NO3)2
(1)从绿色化学的角度分析,___________同学的方案更合理
(2)乙同学实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,宜选择__________装置(填字母序号)。

Ⅱ.某化学实验小组通过实验来探究一包黑色粉是否由Fe3O4、CuO组成探究过程如下:
(1)提出假设:
假设1.黑色粉末是CuO;
假设2.黑色粉末是Fe3O4;
假设3.黑色粉末是CuO和Fe3O4的混合物。
(2)设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
①若假设1成立,则实验现象是溶液显蓝色。
②若假设2或3成立,则实验现象是__________。
为进一步探究,继续向所得溶液加入足量铁粉,若产生_________的现象,则假设3成立。
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。
为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若假设2成立,则产生__________现象;若假设3成立,则产生________现象。
Ⅲ.由Fe3O4、FeO、CuO、Fe组成的固体混合物,在加热条件下用足量的CO还原,得到金属混合物2.86g,将生成的CO2气体用足量的澄清石灰水吸收后,产生5.00g白色沉淀。固体混合物的质量是________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上开学测化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是( )
A.石英溶于烧碱溶液:SiO2+2OH-=SiO32-+H2O
B.氢氧化钠溶液中通入少量的二氧化硫:SO2+OH-=HSO3-
C.碳酸氢钙溶液中加入足量氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O
D.溴化亚铁溶液中通入少量氯气:ZFe2+ +4Br-+3Cl2=2Fe3++2Br2+6Cl-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上开学测化学试卷(解析版) 题型:选择题
一定质量的铜、铝混合物与一定体积硝酸溶液恰好完全反应,得硝酸盐溶液和NO2、N2O4、NO的混合气体,这些气体与标准状况下3.36L氧气混合后通入水中,所有气体恰好完全被水吸收生成硝酸。若向所得硝酸盐溶液中加入NaOH溶液至沉淀最多停止加入,将所产生沉淀滤出,将滤液加水稀释至600ml,此时所得溶液的物质的量浓度为( )
A.1mol/L B.0.5mol/L C.1.2mol/L D.2mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上开学测化学试卷(解析版) 题型:选择题
2013年4月24日,东航首次成功进行了由地沟油生产的生物航空燃油的验证飞行。能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等)的方法是 ( )
A.点燃,能燃烧的是矿物油
B.加入足量氢氧化钠溶液共热,不分层的是地沟油
C.加入水中,浮在水面上的是地沟油
D.测定沸点,有固定沸点的是矿物油
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上开学测化学试卷(解析版) 题型:选择题
只用一种试剂就可以鉴别乙酸溶液、葡萄糖溶液、蔗糖溶液,这种试剂是( )
A.NaOH溶液 B.新制Cu(OH)2悬浊液 C.石蕊试液 D.Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上9月调考化学试卷(解析版) 题型:选择题
80 ℃时,在2 L 密闭容器中充入0.40 mol N2O4,发生反应N2O4(g) 2NO2 (g)ΔH=+Q kJ·mol-1(Q>0),获得如下数据:
2NO2 (g)ΔH=+Q kJ·mol-1(Q>0),获得如下数据:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol·L-1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
下列判断正确的是
A.升高温度该反应的平衡常数K减小
B.20~40 s 内,v(N2O4)=0.004 mol·L-1·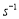
C.100 s 时再通入0.40 mol N2O4,达新平衡时N2O4的转化率增大
D.反应达平衡时,吸收的热量为0.30 Q kJ
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上第一次月考化学试卷(解析版) 题型:选择题
同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3、②NO2进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度为( )

A. ①>② B. ①<② C. ①=② D. 不能确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com