
向amol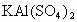 的溶液中逐滴加入
的溶液中逐滴加入 溶液.若已知加入的
溶液.若已知加入的 溶液中含bmol溶质.试讨论:当a和b的比值为何值时,产生的沉淀的成分及其物质的量各为多少?(将结果填入下表).
溶液中含bmol溶质.试讨论:当a和b的比值为何值时,产生的沉淀的成分及其物质的量各为多少?(将结果填入下表).

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:黄冈重点作业 高一化学(下) 题型:013
向含有 的
的 溶液中逐滴加入含amol溶质的NaOH溶液恰好使溶液的pH=7,下列叙述中正确的是
溶液中逐滴加入含amol溶质的NaOH溶液恰好使溶液的pH=7,下列叙述中正确的是
[ ]
A.溶液中
B. mol>沉淀的物质的量>0
mol>沉淀的物质的量>0
C.沉淀的物质的量= mol
mol
D.原溶液中 的物质的量=
的物质的量= mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)向amol NaOH溶液中逐滴加入bmol AlCl3溶液,试回答:
(1)依次写出溶液中发生反应的化学方程式。
(2)若a+b=1,当a取不同值时,生成物可能有以下情况:
①全部是Al(OH)3时,a的取值范围是 。
②全部是NaAlO2时,a的取值范围是 。
③部分是NaAlO2,部分是Al(OH)3,a的取值范围是 。反应所生成的Al(OH)3的物质的量为 mol,反应所生成的各物质的总物质的量(包括水)为 mol(用含b的式子表示)。
④在上述条件下,若要生成7.8g沉淀,则a的值等于 或 。
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com