
【题目】某小组对碳与浓硝酸的反应进行探究,已知:2NaOH+2NO2=NaNO3+NaNO2+H2O,2NaOH+NO2+NO=2NaNO2+H2O。请回答下列可题:
I.甲同学设计 如图所示装置制备并收集NO
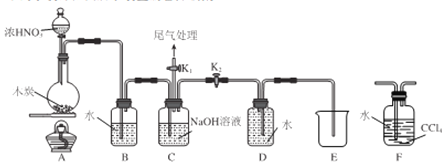
(1)碳与浓硝酸反应的化学方程式为__________________。
(2)C的作用为_______________。
(3)乙同学认为用装置F代替B更合理,理由为_______________。
(4)乙同学用改进后的装置进行实验。
①将浓HNO3滴入圆底烧瓶中的操作为__________________。
②点燃A处酒精灯开始反应后,圆底烧瓶中的现象为________________。
II.探究NO与Na2O2反应
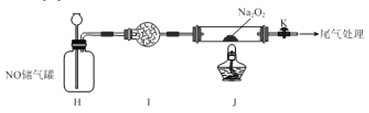
已知NaNO2既有氧化性,又有还原性;J 处硬质玻璃管中制得的NaNO2中含有少量NaNO3。
(5)检验上图装置气密性的方法为____________________。
(6)实验结束后,设计实验证明J 处硬质玻璃管中有NaNO2生成________________。
供选试剂:蒸馏水KI-淀粉溶液,KMnO4溶液、NaOH溶液.BaCl2溶液、稀硫酸
【答案】 C+4HNO3(浓) ![]() 4NO2↑+CO2↑+2H2O 除去反应生成的CO2 装置F可以起到防倒吸的作用 打开分液漏斗玻璃塞(或将分液漏斗玻璃塞的凹槽与分液漏斗口的小孔对准),旋转活塞,使浓硝酸滴入圆底烧瓶 剧烈反应,木炭逐渐减少,液体中有气泡冒出,烧瓶中出现红棕色气体 关闭K,由长颈漏斗向广口瓶中加水至长颈漏斗中的液面高于广口瓶,一段时间后液面差不变则气密性良好 取少量反应后的固体溶于蒸馏水,滴几滴经稀硫酸酸化的KMnO4溶液,溶液褪色则有NaNO2 生成
4NO2↑+CO2↑+2H2O 除去反应生成的CO2 装置F可以起到防倒吸的作用 打开分液漏斗玻璃塞(或将分液漏斗玻璃塞的凹槽与分液漏斗口的小孔对准),旋转活塞,使浓硝酸滴入圆底烧瓶 剧烈反应,木炭逐渐减少,液体中有气泡冒出,烧瓶中出现红棕色气体 关闭K,由长颈漏斗向广口瓶中加水至长颈漏斗中的液面高于广口瓶,一段时间后液面差不变则气密性良好 取少量反应后的固体溶于蒸馏水,滴几滴经稀硫酸酸化的KMnO4溶液,溶液褪色则有NaNO2 生成
【解析】I. (1). 碳与浓硝酸反应生成CO2、NO2和H2O,化学方程式为C+4HNO3(浓) ![]() 4NO2↑+CO2↑+2H2O,故答案为:C+4HNO3(浓)
4NO2↑+CO2↑+2H2O,故答案为:C+4HNO3(浓) ![]() 4NO2↑+CO2↑+2H2O;
4NO2↑+CO2↑+2H2O;
(2). 碳与浓硝酸反应生成的CO2、NO2通入B装置的水中,NO2与水反应生成HNO3和NO,再将混合气体通入装置C的NaOH溶液中,可以除去NO中混有的CO2,故答案为:除去反应生成的CO2;
(3). 将碳与浓硝酸反应生成CO2、NO2通入B装置的水中,因NO2与水反应生成HNO3和NO,造成气体减少、压强减小,从而产生倒吸,若将混合气体通入CCl4中,则不会产生倒吸,故答案为:装置F可以起到防倒吸的作用;
(4). ①. 将分液漏斗中的浓HNO3顺利滴入圆底烧瓶,需先平衡压强,则正确的操作步骤为:打开分液漏斗玻璃塞(或将分液漏斗玻璃塞的凹槽与分液漏斗口的小孔对准),旋转活塞,使浓硝酸滴入圆底烧瓶,并控制滴加速度,故答案为:打开分液漏斗玻璃塞(或将分液漏斗玻璃塞的凹槽与分液漏斗口的小孔对准),旋转活塞,使浓硝酸滴入圆底烧瓶;
②. 向圆底烧瓶中加入浓硝酸后,点燃A处酒精灯,碳与浓硝酸剧烈反应,木炭逐渐减少,液体中有气泡冒出,烧瓶中出现红棕色气体,故答案为:剧烈反应,木炭逐渐减少,液体中有气泡冒出,烧瓶中出现红棕色气体;
II. (5). 检验装置的气密性需先形成密闭体系,正确的方法是:关闭装置后端开关K,由长颈漏斗向广口瓶中加水至长颈漏斗中的液面高于广口瓶,一段时间后液面的高度差不变,则气密性良好,故答案为:关闭K,由长颈漏斗向广口瓶中加水至长颈漏斗中的液面高于广口瓶,一段时间后液面差不变则气密性良好;
(6). J处硬质玻璃管中制得的NaNO2中含有少量NaNO3,因NaNO3在酸性条件下也具有强氧化性,所以不能使用还原性的试剂如KI-淀粉溶液检验,可根据NaNO2具有还原性而NaNO3没有还原性,取少量反应后的固体溶于蒸馏水,滴几滴经稀硫酸酸化的KMnO4溶液,若溶液褪色则有NaNO2生成,故答案为:取少量反应后的固体溶于蒸馏水,滴几滴经稀硫酸酸化的KMnO4溶液,溶液褪色则有NaNO2生成。


科目:高中化学 来源: 题型:
【题目】蛋白质是生命的物质基础。某学习小组通过实验探究一种蛋白质的元素组成。
I.确定该蛋白质中的某些组成元素
(1)为确定该蛋白质中含氮元素,将样品中有机氮转化成铵盐,能证明铵盐存在的实验方法是_________________。
(2)为确定该蛋白质中含碳、氢、硫三种元素,采用如下图装置进行研究,通入氧气使样品在装置A中充分燃烧,并使其产物依次缓缓通过其余装置。
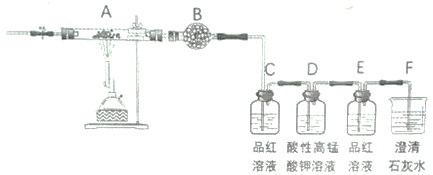
①装置B中的试剂是_________。
②装置D的作用是____________________。
③当装置B、C、E、F依次出现下列现象:________________,品红褪色,______________,出现白色浑浊;可证明燃烧产物中含有H2O、SO2、CO2。
结论:该蛋白质中含碳、氢、硫、氮等元素。
II.为测定该蛋白质中硫元素的质量分数,小组取蛋白质样品充分燃烧,先用足量碘水吸收二氧化硫,再取吸收液,以淀粉为指示剂,用硫代硫酸钠溶液滴定过量的碘。已知:2S2032-+I2=S4062-+2I-
(3)写出二氧化硫与碘水反应的化学方程式:___________________________。
(4)滴定终点的现象为:______________________。
(5)取蛋白质样品mg进行测定,采用C1mol/L的碘水V1mL进行吸收,滴定过量的碘时消耗C2mol/L硫代硫酸钠溶液V2mL。该蛋白质中的硫元素的质量分数为______________。
(6)若燃烧时过量氧气进入吸收液中,可能会导致该蛋白质中的硫元素的质量分数测定值___(填“偏大”或“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银锌蓄电池应用广泛,放电时总反应为Zn+Ag2O2+H2O==Zn(OH)2+Ag2O,某小组以银锌蓄电池为电源,用惰性电极电解饱和Na2SO4溶液制备H2SO4和NaOH,设计如图所示装置。连通电路后,下列说法正确是
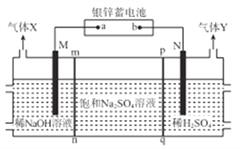
A. 电池的a极反应式为Ag2O2+H2O+2e-=Ag2O+2OH-
B. 气体Y为H2
C. pq膜适宜选择阳离子交换膜
D. 电池中消耗65gZn,理论上生成1mol气体X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
化合物M是合成香精的重要原料。实验室由A和芳香烃E制备M的一种合成路线如下:
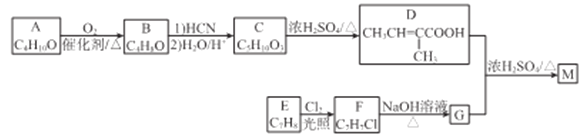
已知: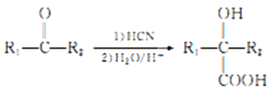 (R1、R2表示烃基或H原子)
(R1、R2表示烃基或H原子)
请回答下列题:
(1)A的化学名称为_________,B的结构简式为________。
(2)C中官能团的名称为________。
(3)D分子中最多有___个原子共平面。
(4)E→F的反应类型为________。
(5)D+G→M的化学方程式为________。
(6)同时满足下列条件的D的同分异构体有___种(不考虑立体异构),其中核磁共振氢谱有3组峰的结构简式为________。
①能发生水解反应和银镜反应; ②不含环状结构
(7)参照上述合成路线和信息。以![]() 为原料(其他无机试剂任选),设计制备
为原料(其他无机试剂任选),设计制备 的合成路线_______________________。
的合成路线_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答下列问题:
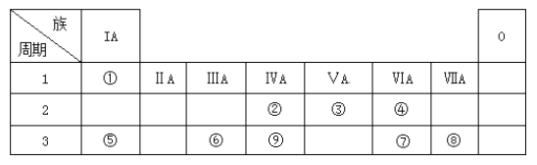
(1)第三周期中元素非金属性最强的元素的原子结构示意图为__________。
(2)②③⑨最高价氧化物对应水化物酸性强弱顺序为(填化学式)_____________。
(3)用电子式表示④的氢化物的形成过程_________________________。
(4)下列可以判断⑤和⑥金属性强弱的是__________。
a. ⑤单质的熔点比⑥单质低
b. ⑤的化合价比⑥低
c. ⑤单质与水反应比单质⑥剧烈
d. ⑤最高价氧化物的水化物的碱性比⑥强
(5)由表中①、③、④、⑥、⑧元素形成的常见物质Z、M、N可发生以下反应:
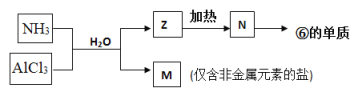
a. M中所含的化学键种类为(若含共价键,请标明极性或非极性)_________。
b. N→⑥的单质的化学方程式_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍及其化合物用途广泛。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,以下是从该矿渣中回收NiSO4的工艺路线:

已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3。锡(Sn)位于第五周期第ⅣA族。
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是______________。
(2)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为______________,“浸渣”的成分除Fe2O3、FeO(OH)外还含有______________(填化学式)。
(3)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入SnCl2将Fe3+还原为Fe2+,所需SnCl2的物质的量不少于Fe3+物质的量的________倍;除去过量的SnCl2后,再用酸性K2Cr2O7标准溶液滴定溶液中的Fe2+,还原产物为Cr3+,滴定时反应的离子方程式为______________。
(4)“浸出液”中c(Ca2+) = 1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-) = ________ mol·L-1。[已知Ksp (CaF2)=4.0×10-11]
(5)本工艺中,萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值是________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
方法a | 用炭粉在高温条件下还原CuO |
方法b | 电解法,反应为2Cu + H2O |
方法c | 用肼(N2H4)还原新制Cu(OH)2 |
(1)已知:2Cu(s)+![]() O2(g)=Cu2O(s)△H =-169kJ·mol-1
O2(g)=Cu2O(s)△H =-169kJ·mol-1
C(s)+![]() O2(g)=CO(g)△H =-110.5kJ·mol-1
O2(g)=CO(g)△H =-110.5kJ·mol-1
Cu(s)+![]() O2(g)=CuO(s)△H =-157kJ·mol-1
O2(g)=CuO(s)△H =-157kJ·mol-1
则方法a发生反应的热化学方程式是_____________________________________。
(2)方法b采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该离子交换膜为______离子交换膜(填“阴”或“阳”),该电池的阳极反应式为______________________________________。
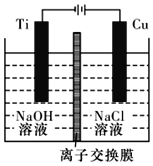
(3)方法c为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2,该制法的化学方程式为________________________________________。
(4)在容积为1L的恒容密闭容器中,用以上方法制得的三种纳米级Cu2O分别进行催化分解水的实验:2H2O(g) ![]() 2H2(g)+O2(g),ΔH>0。水蒸气的浓度c随时间t的变化如下表所示。
2H2(g)+O2(g),ΔH>0。水蒸气的浓度c随时间t的变化如下表所示。
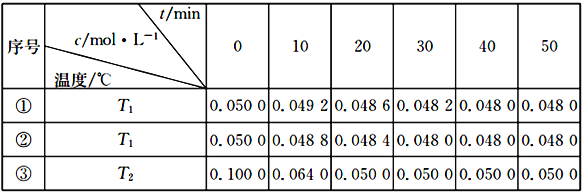
①对比实验的温度:T2_________T1(填“>”、“<”或“=”)
②催化剂催化效率:实验①________实验②(填“>”或“<”)
③在实验③达到平衡状态后,向该容器中通入水蒸气与氢气各0.1mol,则反应再次达到平衡时,容器中氧气的浓度为 ____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com