
| ||
| ||


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源:2014-2015陕西省宝鸡市高一上学期期末化学试卷(解析版) 题型:选择题
通常用于衡量一个国家石油化工发展水平的标志是
A、石油的产量 B、乙烯的产量 C、天然气的产量 D、硫酸的产量
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴彦淖尔市高三上学期期中考试化学试卷(解析版) 题型:选择题
已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列有关叙述正确的是
①生成物的百分含量一定增加 ②生成物的产量一定增加
③反应物的转化率一定增大 ④反应物浓度一定降低
⑤正反应速率一定大于逆反应速率 ⑥使用了合适的催化剂
A.①② B.②⑤ C.⑤ D.④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向浓度为0.1mol/LNaCl、KI混合液中逐滴加入AgNO3溶液 | 出现黄色沉淀 | 溶解性:AgCl>AgI |
| B | 溴乙烷与NaOH的乙醇溶液共热,将溢出气体通入酸性高锰酸钾溶液中 | 溶液紫色褪去 | 证明有乙烯生成 |
| C | 向X的溶液中滴入浓NaOH溶液,将干燥红色石蕊试纸置于管口 | 无明显现象 | X溶液中有NH4+ |
| D | 将SO2气体通入Ba(NO3)2溶液 | 产生白色沉淀 | 沉淀为BaSO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca2+、K+、HCO3-、OH- |
| B、Al3+、NH4+、CO32-、Cl- |
| C、Na+、Ba2+、OH-、NO3- |
| D、H+、NH4+、SO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:

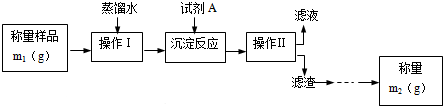
| A、A气体是NH3,B气体是CO2 |
| B、把纯碱及第Ⅲ步所得晶体与某些固体酸性物质(如酒石酸)混合可制泡腾片 |
| C、第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 |
| D、第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铍遇冷水剧烈反应 |
| B、氧化铍的化学式为Be2O3 |
| C、氢氧化铍能与氢氧化钠溶液反应 |
| D、氯化铍水溶液显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com