
【题目】(1)许多运动会使用的火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O过程中的能量变化图,请在图中的括号内填入“+”或“-”。
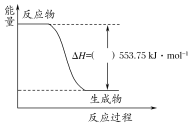
②写出表示丙烷燃烧热的热化学方程式:____________________________________________。
(2)2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=﹣99 kJmol-1。
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=﹣99 kJmol-1。
请回答下列问题:
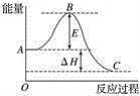
①图中ΔH=______kJmol-1。
②已知单质硫的燃烧热为296 kJmol-1,计算由S(s)生成1 mol SO3(g)的ΔH=______ kJmol-1。
【答案】-C3H8(g)+5O2(g)===3CO2(g)+4H2O(l) ΔH=-2215.0 kJ·mol-1 -198-395
【解析】
(1)①根据图中信息:反应物的能量高于生成物的能量,此反应是放热反应,所以焓变是负值,故答案为:—;
②燃烧热的是指完全燃烧1mol丙烷生成稳定产物二氧化碳气体和液态水所放出的热量,图中是一定量丙烷完全燃烧生成CO2和1mol H2O(l)的能量,1mol丙烷完全燃烧生成CO2和4mol H2O(l)的能量为:553.75kJ/mol×4=2215.0 kJ/mol,所以丙烷燃烧热的热化学方程式为C3H8(g)+5O2(g)═3CO2(g)+4H2O(l) △H=-2215.0 kJ/mol,故答案为:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l) △H=-2215.0 kJ/mol.
(2)因1mol SO2(g)氧化为1mol SO3的△H=-99kJmol-1,所以2molSO2(g)氧化为2molSO3的△H=-198kJmol-1,
则2SO2(g)+O2(g)=2SO3(g)△H=-198kJmol-1,故答案为:-198;
(3)已知①S(s)+O2(g)=SO2(g)△H1=-296KJmol-1,②SO2(g)+![]() O2(g)=SO3(g)△H2=-99kJmol-1;利用盖斯定律将①×3+②×3可得S(s)+3/2O2(g)=SO3(g)△H=-395kJmol-1,故答案为: -395。
O2(g)=SO3(g)△H2=-99kJmol-1;利用盖斯定律将①×3+②×3可得S(s)+3/2O2(g)=SO3(g)△H=-395kJmol-1,故答案为: -395。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案科目:高中化学 来源: 题型:
【题目】利用如图所示装置测定中和热的实验步骤如下:

①用量筒量取50mL0.50mol·L-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50mL0.55mol·L-1NaOH溶液,并用另一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度,回答下列问题:
(1)为什么所用NaOH溶液要稍过量____________________。
(2)倒入NaOH溶液的正确操作是________(填序号)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是________(填序号)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L1mol·L-1的稀盐酸恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2、△H3的大小关系为________。
(5)________(填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于甲烷、乙烯、苯三种烃的比较中,正确的是![]()
![]()
A. 只有甲烷不能因化学反应而使酸性高锰酸钾溶液褪色
B. 除甲烷外,其余两种分子内所有原子都共平面
C. 甲烷和苯属于饱和烃,乙烯是不饱和烃
D. 在空气中分别完全燃烧等质量的这三种烃,苯消耗的氧气最多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化规律正确的是( )
A.Na、Mg、Ca原子半径从大到小B.HCl、PH3、H2S热稳定性从弱到强
C.Al、Ca、K还原性从弱到强D.H3PO4、H2SO4、HClO4酸性从弱到强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2H2O(g)===2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1 ②H2S(g)===H2(g)+S(g) ΔH=+20.1 kJ·mol-1下列判断正确的是( )
A. 氢气的燃烧热:ΔH=-241.8 kJ·mol-1
B. 相同条件下,充分燃烧1 mol H2(g)与1 mol S(g)的混合物比充分燃烧1 mol H2S(g)放热多20.1 kJ
C. 由①②知,水的热稳定性小于硫化氢
D. ②中若生成固态硫,ΔH将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为800 oC时A、B、C三种气体在密闭容器中反应时浓度的变化,分析图像得出的结论错误的是( )
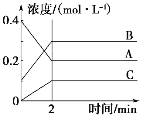
A. A是反应物
B. 前2 min A的反应速率为0.1 mol·L-1·min-1
C. 2min后反应达到平衡,v(A)正 = v(C)逆
D. 反应的方程式为2A(g)![]() 2B(g)+C(g)
2B(g)+C(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲萘醌(维生素K)有止血作用,它可通过2—甲基萘的氧化而制得,反应中常用乙酸作催化剂,该反应放热,可表示为:
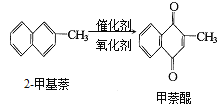
在某次合成反应中,用1.4g的2—甲基萘,才制得0.17g甲萘醌,已知该次合成反应的速率是快的,试判断导致其产率低的原因是
A.使用了过量的氧化剂 B.没有用乙酸,而是使用了其它催化剂
C.把反应混合物加热 D.所生成的甲萘醌是沉淀物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应A(g)+B(g)![]() 2C(g),已知1molA与1molB反应达平衡时生成0.4molC.
2C(g),已知1molA与1molB反应达平衡时生成0.4molC.
(1)同温同压下,2molA与2molB反应达平衡时生成_______molC。
(2)恒温恒容下,2molA与2molB反应达平衡时生成_______molC。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com