
【题目】硅、硼、铜、硒的单质及化合物在现代工业生产中有着广泛应用。回答下列问题:
(1)基态Cu+的核外价层电子排布式为_______________;Be、B、Al的第一电离能由大到小的顺序是______________________________。
(2)硒、硅均能与氢元素形成气态氢化物,若“Si-H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se___ Si(填“>”、“<”)。
(3)SeO32-中Se原子的杂化类型为______,与其互为等电子体的一种分子的分子式是______________。
(4)CuSO4和Cu(NO3)2是自然界中重要的铜盐,向CuSO4熔液中加入过量稀氨水,产物的外界离子的空间构型为_________,Cu(NO3)2中的化学键除了σ键外,还存在_______________。
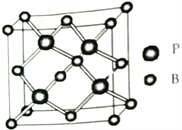
(5)磷化硼(BP)是一种耐磨材料,熔点高,其晶胞结构如图所示。该晶胞中B的堆积方式为___________,己知该晶体的晶胞参数a pm,用NA代表阿伏加德罗常数的值,则该晶体的密度为____ g·cm-3;构成晶体的两种粒子之间的最近距离为__________pm。
【答案】 3d10 Be> B>Al > sp3 NF3(或PF3、NCl3、PCl3等) 正四面体 离子键、π键 面心立方最密堆积 ![]()
![]()
【解析】(1)Cu的原子序数为29,核外电子数为29,Cu的核外电子排布式为[Ar]3d104s1,失去4s上的一个电子后,基态Cu+的核外价层电子排布式为3d10;Be和B处于同一周期,同一周期自左向右第一电离能有增大的趋势,但Be的4s能级处于全充满状态,稳定性强,故第一电离能Be>B,B和Al处于同一主族,同一主族自上而下第一电离能逐渐减小,即B>Al,所以第一电离能由大到小的顺序是Be>B>Al。本题答案为:3d10 ; Be>B>Al。
(2)“Si-H”中共用电子对偏向氢元素,说明非金属性H>Si,氢气与硒反应时单质硒是氧化剂,说明非金属性Se>H,即非金属性Se> Si,非金属性越强电负性越大,则硒与硅的电负性相对大小为Se>Si。
(3)SeO32-中Se原子孤对电子对数=![]() =1,σ键个数=3,所以为Se原子 sp3 杂化;SeO32-价电子总数为26,通过增减Se和O的电子数,进行判断,与其互为等电子体的一种分子的分子式可以是 NF3(或PF3、NCl3、PCl3等)。
=1,σ键个数=3,所以为Se原子 sp3 杂化;SeO32-价电子总数为26,通过增减Se和O的电子数,进行判断,与其互为等电子体的一种分子的分子式可以是 NF3(或PF3、NCl3、PCl3等)。
(4)SO42-中心原子的孤电子对数=![]() =0,含4个σ键,为sp3 杂化,空间构型为正四面体;Cu(NO3)2中的化学键除了σ键外,Cu2+与NO3-之间存在离子键,NO3-中存在π键。
=0,含4个σ键,为sp3 杂化,空间构型为正四面体;Cu(NO3)2中的化学键除了σ键外,Cu2+与NO3-之间存在离子键,NO3-中存在π键。
(5)从晶胞结构图看出,该晶胞中B的堆积方式为面心立方最密堆积;一个晶胞中B原子的数目=1(8个顶点)+3(6个面心)=4,P原子的数目=4(4个体心),1mol晶胞质量=(11+31)×4g=168g,1mol晶胞体积=(a×10-10)3NA,根据ρ=m/V,则该晶体的密度为![]() g·cm-3;仔细观察BP的晶胞结构不难发现,P位于BP晶胞中8个小立方体中互不相邻的4个小立方体的体心,B与P间的距离就是小立方体对角线的一半,即
g·cm-3;仔细观察BP的晶胞结构不难发现,P位于BP晶胞中8个小立方体中互不相邻的4个小立方体的体心,B与P间的距离就是小立方体对角线的一半,即![]() ×
×![]()
![]() pm。
pm。


科目:高中化学 来源: 题型:
【题目】下列物质的名称或俗名与化学式相对应的是
A.小苏打——Na2CO3B.火碱——Na2O2
C.生石灰——Ca(OH)2D.醋酸——CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,向Al2O3和过量C粉的混合物中通入氯气,可制得易水解的AlCl3,实验装置如图所示。下列说法不正确的是
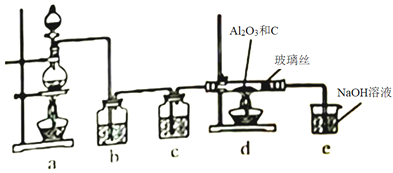
A. c中盛装的是浓硫酸
B. 实验时应先点燃d处酒精灯,再点燃a处酒精灯
C. 此反应中的尾气,除氯气外都可直接排放到大气中
D. 该装置不完善,其中应改进的一项是在d、e之间添加一个干燥装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铁锂是锂电池的电极材料,其成分为LiFePO4、 碳粉和铝箔。对该材料进行资源回收研究,设计实验流程如下:
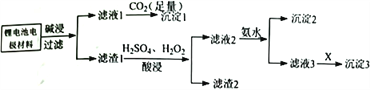
已知:溶解度表:
Li2CO3 | LiOH | LiI | |
0℃ | l.54g | 12.7g | 151g |
100℃ | 0.72g | 13.6g | 179g |
回答下列问题:
(1)由滤液1到沉淀1反应的离子方程式为_______________________________。
(2)向滤渣1加入H2SO4、H2O2混合溶液时,磷酸铁锂溶解,反应的离子方程式为__________________________________。
(3)对滤渣1酸浸操作,下列实验条件控制正确的是(填字母代号) _________________。
a.加入H2O2溶液适当过量,有利于滤渣1的转化
b.适当提高硫酸溶液浓度并搅拌
c.用HNO3代替所加H2SO4和H2O2,节约药品更环保
(4)滤液2加氨水时,调节pH=3,此时溶液中c(Fe3+)=________ (常温下,Ksp[Fe(OH)3]=4.0×10-38)。
(5)向滤液3中加入物质X,根据溶解度表判断X可能是:___________ (填Na2CO3、NaOH或Nal)。
(6)对沉淀3进行洗涤操作,应选择________(选填“冷水”或“热水”)进行洗涤。
(7)磷酸铁锂电池的工作原理为:LiFePO4+ 6C![]() Li1-xFePO4 +LixC6,电池中的电解质可传导Li+。放电时正极的电极反应式为________________________________。
Li1-xFePO4 +LixC6,电池中的电解质可传导Li+。放电时正极的电极反应式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氯的说法不正确的是( )
A.氯气是由瑞典化学家舍勒首先制得B.氯气是由英国化学家戴维命名的
C.氯元素主要以单质的形式大量存在海水里D.氯气是一种重要的化工原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
元素 | 相关信息 |
X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
Z | Z和Y同周期,Z的电负性大于Y |
W | W的一种核素的质量数为63,中子数为34 |
(1)Y位于元素周期表第________周期第________族,Y和Z的最高价氧化物对应的水化物的酸性较强的是________(写化学式)。
(2)W的基态原子核外电子排布式是___________________________________。
(3)W2Y在空气中煅烧生成W2O的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学科技工作者对含有碳杂质的金属铝的腐蚀与溶液酸碱性的关系进行了研究,在25℃时得出溶液pH值对铝的腐蚀影响关系如图所示,下列说法正确的是( )
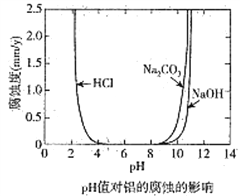
A. 金属铝在浓硫酸中的腐蚀速率大于盐酸中的腐蚀速率
B. 金属铝在中性环境中不易被腐蚀
C. 金属铝在pH=8.5的Na2CO3溶液中会发生电化学腐蚀析出氧气
D. 不能用电解的方法在金属铝的表面生成致密的氧化物薄膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨晶体结构中的某一种的某一部分。
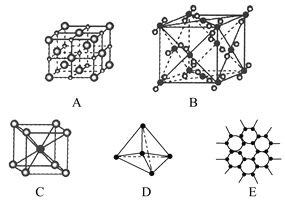
(1)其中代表金刚石的是(填编号字母,下同)________,其中每个碳原子与________个碳原子最接近且距离相等。金刚石属于________晶体。
(2)其中代表石墨的是_______,其中每个正六边形占有碳原子数平均为________个。
(3)其中代表NaCl晶体的是________,每个Na+周围与它最接近且距离相等的Na+有________个。
(4)代表CsCl晶体的是________,它属于________晶体,每个Cs+与________个Cl-紧邻。
(5)代表干冰的是________,它属于________晶体,每个CO2分子与________个CO2分子紧邻。
(6)上述五种物质熔点由高到低的排列顺序为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com