


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaH2PO4的水解:H2PO4-+H2O?H3O++HPO42- |
| B、H2S在水中的电离:H2S?2H++S2- |
| C、Na2SO3的水解:SO32-+H2O?HSO3-+OH- |
| D、CH3COONa在水中的电离:CH3COONa?CH3COO-+Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③⑤ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
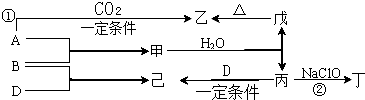
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量的浓盐酸与MnO2反应 |
| B、过量的Zn与18 mol/L的硫酸反应 |
| C、过量的Fe与稀硝酸反应 |
| D、过量的H2与N2在催化剂存在下反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com