
| A. | 甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色 | |
| B. | 苯酚能跟NaOH溶液反应,而乙醇不能与NaOH溶液反应 | |
| C. | 苯与硝酸在加热的条件生成硝基苯,而甲苯在加热条件下与硝酸发生反应生成三硝基甲苯 | |
| D. | 乙炔能发生加成,乙烷不能 |
分析 A.苯环影响甲基,甲苯易被氧化;
B.苯环影响-OH,具有酸性;
C.甲苯与硝酸反应更容易,说明甲苯中苯环上H原子更活泼;
D.乙炔中含官能团碳碳三键,乙烷中不含官能团.
解答 解:A.苯不能使酸性高锰酸钾溶液褪色,苯上没有可以被氧化的氢原子;甲苯能使高锰酸钾酸性溶液褪色,说明苯环的影响使侧链甲基易被氧化,故A不选;
B.苯环影响-OH,具有酸性,乙醇为中性,-OH连接的烃基不同,可说明或原子与原子团间的相互影响会导致物质的化学性质不同,故B不选;
C.甲基影响苯环,则甲苯中苯环上的H易被取代,甲苯苯环上氢原子比苯分子中的氢原子易被溴原子取代,可说明或原子与原子团间的相互影响会导致物质的化学性质不同,故C不选;
D.乙炔中含官能团碳碳三键,乙烷中不含官能团,因官能团不同导致化学性质不同,故D选.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、原子或原子团的相互影响为解答的关键,侧重常见有机物结构、性质的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
| A. | 铁与盐酸反应生成氯化铁和氢气 | |
| B. | 铁在高温下与水蒸气的反应是置换反应 | |
| C. | 铁与盐酸、水蒸气反应,均作还原剂 | |
| D. | 铁丝在空气、纯氧中均不能燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3的水解:HCO3-+H2O?H3O++CO32- | |
| B. | 醋酸铵的电离:CH3COONH4?CH3COO-+NH4+ | |
| C. | 汽车尾气净化反应2NO+2CO=2CO2+N2能够自发进行,则该反应的△H>0 | |
| D. | 碳在高温下还原二氧化硅SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③⑤⑦ | C. | ②③⑥ | D. | ③④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S?2H++S2- | B. | NaHSO4═Na++H++SO42- | ||
| C. | CO32-+2H2O?H2CO3+2OH- | D. | Al3++3H2O?Al(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
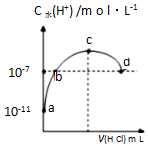 常温下,向20mL 0.1mol•L-1氨水溶液中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示.则下列说法正确的是( )
常温下,向20mL 0.1mol•L-1氨水溶液中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示.则下列说法正确的是( )| A. | 常温下,0.1mol•L-1氨水的电离常数K约为1×10-5mol•L-1 | |
| B. | a、b之间的点一定满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| C. | c点溶液中c(NH4+)=c(Cl-) | |
| D. | d点代表两溶液恰好完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
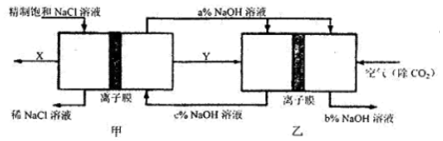
| A. | 甲装置为电解池,其左室为阴极室 | |
| B. | 甲乙两装置中使用的均为阳离子交换膜 | |
| C. | 乙装置为燃料电池,其左室反应为H2-2e-═2H+ | |
| D. | 图中三种NaOH溶液的质量分数关系为b%>c%>a% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1<0△H3>0 | B. | △H5<0△H4<△H3 | C. | △H1=△H2+△H3 | D. | △H3=△H4+△H5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com