
【题目】a、b、c、d、e、f是原子序数依次递增的短周期元素,周期表中b与c、c与d相邻;b与f的最外层电子数之比为2:3,c的最外层电子数比f的最外层电子数少1个;常见化合物e2d2与水反应生成d的单质;a与d两元素只能形成两种化合物,电子数分别为10和18个。
(1)b、c、d氢化物稳定性顺序为(用分子式表示)______<______<______;
(2)由4个a原子、2个c、3个d原子组成化合物Z,则Z中的化学键类型为______;
(3)bc-离子的电子式为____________;
(4)一定量的e2d2与bd2反应后的固体物质,恰好与0.8 mol稀盐酸溶液完全反应,并收集到0.25 mol气体,则该固体物质的组成为_______mol Na2O2、________mol Na2CO3。
【答案】CH4<NH3<H2O 共价键和离子键![]() 0.3 mol Na2O20.1 mol Na2CO3
0.3 mol Na2O20.1 mol Na2CO3
【解析】
a、b、c、d、e、f是原子序数依次递增的短周期元素,常见化合物e2d2与水反应生成d的单质,所以d是O,e是Na;a与d两元素只能形成两种化合物,电子数分别为10和18个,a是H,形成的化合物分别是水和双氧水。周期表中b与c、c与d相邻,根据原子序数关系可知b是C,c是N;b与f的最外层电子数之比为2:3,c的最外层电子数比f的最外层电子数少1个,所以f是S,据此解答。
根据以上分析可知a是H,b是C,c是N,d是O,e是Na,f是S,则
(1)非金属性越强,氢化物越稳定,非金属性C<N<O,则b、c、d氢化物稳定性顺序为CH4<NH3<H2O;
(2)由4个a原子、2个c、3个d原子组成化合物Z是硝酸铵,含有化学键类型为共价键和离子键;
(3)bc-离子的化学式为CN-,根据氮气的电子式可知其电子式为![]() ;
;
(4)一定量的Na2O2与CO2反应后的固体物质为碳酸钠或碳酸钠和过氧化钠,恰好与0.8 mol稀盐酸溶液完全反应,并收集到0.25 mol气体,设固体物质中碳酸钠是x mol,过氧化钠是y mol,则根据钠离子、氯离子守恒可知2x+2y=0.8,产生的气体是二氧化碳和氧气,则x+0.5y=0.25,解得x=0.1,y=0.3。即该固体物质的组成为0.3 mol Na2O2、0.1 mol Na2CO3。


科目:高中化学 来源: 题型:
【题目】某同学用以下装置制备并检验Cl2的性质。下列说法正确的是( )

A. Ⅰ图:若MnO2过量,则浓盐酸可全部消耗完
B. Ⅱ图:证明新制氯水具有酸性和漂白性
C. Ⅲ图:产生了棕黄色的雾
D. Ⅳ图:有色布条均褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用离子方程式解释下列问题
(1)A12S3为什么不能用Na2S溶液和A1C13溶液制备_____________________________________。
(2)泡沫灭火器原理_____________________________________。
(3)氯化铁溶液蒸干并灼烧的产物是________________________,原因是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于“摩尔”的理解不正确的是( )
A.摩尔是一个物理量
B.摩尔是物质的量的单位,简称摩,符号为mol
C.1mol12C与0.012kg12C所含碳原子数相同
D.1molO2约含6.02×1023个氧分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛(HCHO)与葡萄糖相似具有强还原性,40%甲醛溶液沸点为96℃,易挥发。为探究过量甲醛和新制Cu(OH)2反应的产物,进行如下研究。
(1)在如图装置中进行实验,向a中加入0.5 mol/LCuSO4溶液50 mL和5 mol/LNaOH溶液100 mL,振荡,再加入40%的甲醛溶液50 mL,缓慢加热a,在65 ℃时回流20分钟后冷却至室温。反应过程中观察到有棕色固体生成,最后变成红褐色,并有气体产生。

①仪器b的名称是_________,作用为_________。
②能说明甲醛具有还原性的实验现象是______________。
(2)查阅资料发现气体产物是副反应产生的。为确认气体产物含H2不含CO,将装置A和如图所示的装置连接后进行实验。
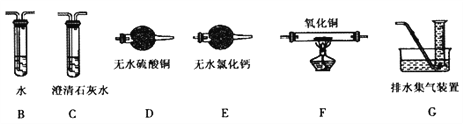
依次连接的合理顺序为A→B→___→_____→_____→_____→G,__________装置B的作用是______。
(3)已知:![]() 。设计实验证明a中甲醛的碳元素未被氧化成+4 价,___________。
。设计实验证明a中甲醛的碳元素未被氧化成+4 价,___________。
(4)为研究红色固体产物的组成,进行如下实验(以下每步均充分反应):
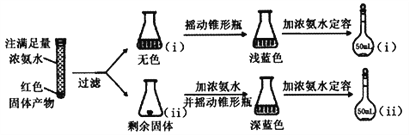
已知:Cu2O ![]() [Cu(NH3)4]+(无色)
[Cu(NH3)4]+(无色)![]() [Cu(NH3)4]2+(蓝色)
[Cu(NH3)4]2+(蓝色)
①摇动锥形瓶i的目的是__________。
②锥形瓶ii中固体完全溶解得深蓝色溶液的离子方程式为_______________。
③将容量瓶ii中的溶液稀释100倍后,溶液的颜色与容量瓶i相近。由此可知固体产物的组成及物质的量之比约为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年中国药学家屠呦呦获得诺贝尔医学奖,以表彰她在青蒿素研究方面做出的突出贡献。提取青蒿素通常可以用乙醚浸取,这与下列哪种方法的原理相同
A.蒸馏法B.过滤法C.结晶法D.萃取法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸的反应为:S+2KNO3+3C![]() K2S+N2↑+3CO2↑,下列说法中正确的是 ( )
K2S+N2↑+3CO2↑,下列说法中正确的是 ( )
A. 该反应中的还原剂为KNO3
B. 该反应中C被还原
C. 若消耗32g S,该反应转移电子数为2 NA
D. 若生成标准状况下气体22.4L,则有0.75 mol物质被还原
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com