
·ÖĪö øł¾ŻĮņ»ÆŃĒĢśµÄČܶȻż³£ŹżŗĶŃĒĢśĄė×ÓÅØ¶Č¼ĘĖćĮņĄė×ÓÅØ¶Č£¬ŌŁøł¾ŻĒāĮņĖįµÄµēĄėĘ½ŗā³£Źż¼ĘĖćĒāĄė×ÓÅØ¶Č£¬×īŗóĄūÓĆpH¼ĘĖć¹«Ź½¼ĘĖćČÜŅŗµÄpH£®
½ā“š ½ā£ŗ½«ŹŹĮæFeS Ķ¶ČėH2S ±„ŗĶČÜŅŗÖŠ£¬ÓūŹ¹ČÜŅŗÖŠc£ØFe2+£©“ļµ½1mol/L£¬ŌņČÜŅŗÖŠc£ØS2-£©=$\frac{{K}_{sp}}{c£ØF{e}^{2+}£©}$=$\frac{6.25”Į1{0}^{-18}}{1}$mol/L=6.25”Į10-18mol/L£¬
øł¾Żc2£ØH+£©•c£ØS2-£©=1.0”Į10-22æÉÖŖ£ŗc£ØH+£©=$\sqrt{\frac{1”Į1{0}^{-22}}{6.25”Į1{0}^{-18}}}$mol/L=4”Į10-3mol/L£¬
ĖłŅŌÓ¦µ÷½ŚČÜŅŗµÄpH=-lg4”Į10-3=3-2lg2=2.4£¬
¹Ź“š°øĪŖ£ŗ2.4£®
µćĘĄ ±¾Ģāæ¼²éĮĖpH¼ĘĖć”¢ÄŃČÜĪļČܶȻż³£ŹżµÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬øł¾ŻČܶȻż³£Źż¼°ČõĖįµÄµēĄėĘ½ŗā³£Źż½ųŠŠČÜŅŗµÄpH¼ĘĖćŹĒ½ā“šµÄ¹Ų¼ü£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°»Æѧ¼ĘĖćÄÜĮ¦£®


 ĒįĖÉæĪĢƵ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
ĒįĖÉæĪĢƵ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
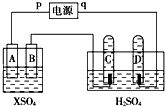 ČēĶ¼£¬p”¢qĪŖÖ±Į÷µēŌ“µÄĮ½¼«£¬AÓÉ+2¼Ū½šŹōµ„ÖŹXÖĘ³É£¬B”¢C”¢DĪŖ²¬µē¼«£¬½ÓĶصēŌ“£¬½šŹōX³Į»żÓŚB¼«£¬Ķ¬Ź±C”¢D¼«ÉĻ¾ł²śÉśĘųÅŻ£¬ŹŌ»Ų“š£ŗ
ČēĶ¼£¬p”¢qĪŖÖ±Į÷µēŌ“µÄĮ½¼«£¬AÓÉ+2¼Ū½šŹōµ„ÖŹXÖĘ³É£¬B”¢C”¢DĪŖ²¬µē¼«£¬½ÓĶصēŌ“£¬½šŹōX³Į»żÓŚB¼«£¬Ķ¬Ź±C”¢D¼«ÉĻ¾ł²śÉśĘųÅŻ£¬ŹŌ»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ā±ĖŲµ„ÖŹµÄ×īĶā²ćµē×ÓŹż¶¼ŹĒ7 | |
| B£® | Ā±ĖŲµ„ÖŹÓėH2»ÆŗĻµÄČŻŅ׳Ģ¶ČĪŖF2£¼Cl2£¼Br2£¼I2 | |
| C£® | Ā±ĖŲµ„ÖŹÓėH2»ÆŗĻµÄ²śĪļÓÉÉĻÖĮĻĀĪČ¶ØŠŌ¼õČõ£¬ĘäĖ®ČÜŅŗµÄĖįŠŌŌöĒæ | |
| D£® | “ÓFµ½I£¬ŌŖĖŲ·Ē½šŹōŠŌŅĄ“Ī¼õČõ£¬ŌņĘä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŅĄ“Ī¼õČõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Ļ”ŃĪĖį | B£® | Na2SO4¾§Ģå | C£® | KNO3¾§Ģå | D£® | FeCl3¾§Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ź±¼ä£Øs£© C£Ømol/L£© | 0 | 20 | 40 | 60 | 80 | 100 |
| C£ØN2O4£© | 0.20 | a | 0.10 | c | d | e |
| C£ØNO2£© | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĢśŗĶĻ”ĮņĖį·“Ó¦£ŗ2Fe+6H+ØT2Fe3++3H2”ü | |
| B£® | NaHCO3ČÜŅŗÓėNaOHČÜŅŗ·“Ó¦£ŗOH-+HCO3-ØTCO32-+H2O | |
| C£® | ÄĘŗĶĄäĖ®·“Ó¦£ŗNa+2H2OØTNa++2OH-+H2”ü | |
| D£® | ĀČ»ÆĀĮČÜŅŗÖŠ¼ÓČė¹żĮæµÄ°±Ė®£ŗAl3++4NH3•H2OØTAlO2-+4NH4++2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬H2£Øg£©+Cl2£Øg£©=2HCl£Øg£©ŌŚ¹āÕÕŗĶµćČ¼Ģõ¼žĻĀµÄ”÷HĻąĶ¬ | |
| B£® | µČÖŹĮæµÄĮņÕōĘųŗĶĮņ¹ĢĢå·Ö±šĶźČ«Č¼ÉÕ£¬ŗóÕ߷ųöµÄČČĮæ¶ą | |
| C£® | ŌŚ¼ÓČČĢõ¼žĻĀ·¢ÉśµÄ·“Ó¦¾łĪŖĪüČČ·“Ó¦ | |
| D£® | ĪļÖŹ·¢Éś»Æѧ·“Ó¦Ź±²»Ņ»¶Ø¶¼°éĖę×ÅÄÜĮæ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÖŹ×ÓŹż | B£® | ÖŹĮæŹż | C£® | ÖŠ×ÓŹż | D£® | µē×ÓŹż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā

| A£® | Fe2+”¢I-”¢Cl-ČżÖÖĄė×ÓŅ»¶Ø“ęŌŚ | |
| B£® | ²»ÄÜČ·¶ØNa+ŗĶCl-ŹĒ·ń“ęŌŚ£¬CO${\;}_{3}^{2-}$Ņ»¶Ø²»“ęŌŚ | |
| C£® | Fe3+ÓėFe2+ÖĮÉŁÓŠŅ»ÖÖ | |
| D£® | øĆČÜŅŗÖŠc£ØCl-£©”Ż0.1mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com