
短周期元素X原子核外的电子处于n个电子层上,最外层电子数为(2n+1),核内质子数为(2n2-1)。有关X的说法中不正确的是 ( )
A.X元素气态氢化物的水溶液不可能呈酸性
B.X能形成化学式为NaXO3的含氧酸钠盐
C.X原子的最外层电子数和核电荷数不可能为偶数
D.X元素常见单质的化学式为X2
科目:高中化学 来源: 题型:
某有机物X的结构简式如下图所示,则下列有关说法中正确的是 ( )
A.X的分子式为C12H16O3
B.X在一定条件下能发生加成、加聚、取代、消去等反应
C.在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成
D.可用酸性高锰酸钾溶液区分苯和X
查看答案和解析>>
科目:高中化学 来源: 题型:
透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶。制备它的一种配方中含有下列四种物质:
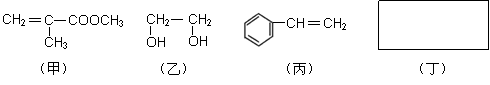 |
(1)丙的名称是____________;乙中官能团的名称是 。
(2)写出甲和丙聚合得到高聚物的结构简式 。
(3)化合物丁的分子式为C6H6O2,只含两种化学环境的氢原子,遇FeCl3溶液呈现特征颜色。写出丁与足量碳酸钠溶液反应的化学方程式 。
(4)下列试剂中与上述四种物质都能发生反应的是___________(填写编号)。
a. Br2的CCl4溶液 b. 石蕊溶液 c. 酸性KMnO4溶液 d. O2
查看答案和解析>>
科目:高中化学 来源: 题型:
为解决日益加剧的温室效应等问题,科学家正在研究建立如下图所示的二氧化碳新循
环体系:
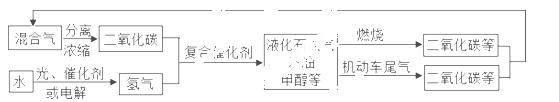
上述关系图能反映的化学观点或化学思想有:( )
①化学变化中元素种类是守恒的;②燃烧时化学能可以转化为热能和光能;③光能或电能可以转化为化学能;④无机物和有机物可以相互转化;⑤二氧化碳也是一种重要的资源.
A.①②③ B.①②④⑤ C.①④⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
有 X和
X和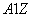 X+两种粒子,下列叙述正确的是 ( )
X+两种粒子,下列叙述正确的是 ( )
A.一定都是由质子、中子、电子组成的
B.化学性质几乎完全相同
C.质子数一定相等,质量数和中子数一定不相等
D.核电荷数和核外电子数一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
现有部分元素的性质与原子(或分子)结构如下表:
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子 |
| Y | M层比K层少1个电子 |
| Z | 第三周期元素的简单阳离子中半径最小 |
(1)写出元素T的原子结构示意图:_______________________________________ .
.
(2)元素Y与元素Z相比,金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________(填序号).
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈
d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既含离子键又含非极性共价键的化合物,写出该化 合物的电子式:_________________________________________________.
合物的电子式:_________________________________________________.
(4)元素T和元素X以原子个数比2∶1化合形成化合物Q,元素X与氢元素 以原子个数比1∶2化合形成常用于火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式___________________________.
以原子个数比1∶2化合形成常用于火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式___________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如
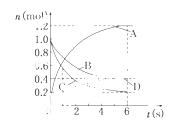 图所示,对该反应的推断合理的是 ( )
图所示,对该反应的推断合理的是 ( )
A.该反应的化学方程式为3B+4D 6A+2C
6A+2C
B.反应进行到1 s 时,v(A)=v(D)
时,v(A)=v(D)
C.反应进行到6 s时,B的平均反应速率为0.05 mol/(L·s)
D.反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵在 500℃时隔绝空气加热完全分解。回答下列问题:
(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和 。
(2)为检验分解产物的成份,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。
① A中固体充分加热较长时间后,通入氮气,目的是 。
②为验证A中残留物是否含有FeO,需要选用的试剂有 。
A.KSCN溶液 B.稀硫酸
C.浓盐酸 D.KMnO4溶液
③装置B中BaCl2溶液的作用是为了检验分解产物中是否有 气体生成,若含有该气体,观察到的现象为 。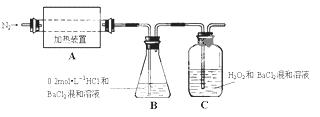
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,则b a(填“大于”、“小于”或“等于”)
⑤实验中,观察到C中有白色沉淀生成,则C中发生的反应为
(用离子方程式表示)。
(3)已知亚铁离子被氧气氧化的反应是:4Fe2+ + O2 + (4+2x) H2O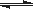 2Fe2O3•xH2O + 8H+,硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
2Fe2O3•xH2O + 8H+,硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是 ( )
A.原子半径的大小顺序:r(Y)>r(Z)>r(W)
B.元素Z、W的简单离子的电子层结构不同
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com