
| A. | 在水溶液中能电离出H+的化合物都是酸 | |
| B. | 强电解质溶液导电能力强,弱电解质溶液导电能力弱 | |
| C. | 金属氧化物不一定是碱性氧化物,碱性氧化物一定是金属氧化物 | |
| D. | 酸碱盐都是电解质,其电离的过程属于化学变化 |
分析 A.在水溶液中能电离出的阳离子全部是H+的化合物属于酸;
B.溶液的导电能力与溶液电荷浓度有关,与电解质的强弱无关;
C.碱性氧化物一定为金属氧化物,而金属氧化物不一定为碱性氧化物,如过氧化钠不属于碱性氧化物;
D.电解质是指:在水溶液中或熔融状态下能够导电的化合物,非电解质是在水溶液中和熔融状态下都不能够导电的化合物,化学变化实质是旧键断裂和新键形成.
解答 A.只有在水溶液中能电离出的阳离子全部是H+的化合物才属于酸,如硫酸氢钠在水溶液中能电离出氢离子,但是属于盐,故A错误;
B.溶液的导电能力与溶液电荷浓度有关,与电解质的强弱无关,如AgCl为强电解质,但溶液的导电性很弱,故B错误;
C.碱性氧化物对应的水化物为碱,所以碱性氧化物一定是金属氧化物,而金属氧化物不一定是碱性氧化物,如过氧化钠为金属氧化物,但是过氧化钠不属于碱性氧化物,故C正确;
D.酸碱盐都是电解质,其电离的过程无新的化学键形成不属于化学变化,故D错误;
故选C.
点评 本题考查了电解质电离、酸碱盐、氧化物的概念,题目难度中等,注意掌握碱性氧化物的概念与判断方法,明确物质溶解为物理变化,掌握基础是解题关键.


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:选择题
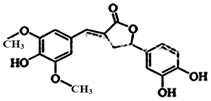 图示为一种天然产物,具有一定的除草功效,下列有关该化合物的说法正确的是( )
图示为一种天然产物,具有一定的除草功效,下列有关该化合物的说法正确的是( )| A. | 分子中含有三种官能团 | |
| B. | 1 mol 该化合物最多能与6 mol NaOH 反应 | |
| C. | 既可以发生取代反应,又能够发生加成反应 | |
| D. | 既能与FeCl3发生显色反应,也能和NaHCO3反应放出CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 温度/℃ | SO2/mol | O2/mol | 催化剂 |
| A | 400 | 4 | 2 | 无 |
| B | 400 | 2 | 1 | 无 |
| C | 500 | 2 | 1 | 无 |
| D | 500 | 4 | 2 | 有 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2HClO=2HCl+O2↑ | B. | Zn+CuSO4=Cu+ZnSO4 | ||
| C. | 2NaOH+H2SO4=Na2SO4+2H2O | D. | H2+F2=2HF |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
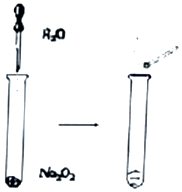 Na2O2具有强氧化性,可以用来漂白纺织累物品、麦秆、纤维等.
Na2O2具有强氧化性,可以用来漂白纺织累物品、麦秆、纤维等.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙与盐酸的反应:CO32-+2H+═CO2↑+H2O | |
| B. | 澄清石灰水中通入过量CO2:CO2+OH-═HCO3- | |
| C. | 钠与水的反应:2Na+2H2O═2Na++OH-+H2↑ | |
| D. | 铁和稀硫酸反应:2Fe+6H+═3Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L二氧化硫所含的氧原子数等于NA | |
| B. | 0.5molH2O所含的电子数为9NA | |
| C. | 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA | |
| D. | 300mL2mol•L-1蔗糖溶液中所含分子数为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,某溶液中由水电离出来的 c(H+)=1×10-amol•L-1,若 a<7,则该溶液可能为 NaHSO4溶液 | |
| B. | 中和同体积、同 pH 的硫酸、盐酸和醋酸所需相同浓度的 NaOH 溶液的体积关系:V(硫酸)>V(盐酸)>V(醋酸) | |
| C. | 向 AgCl 悬浊液中加入 NaCl 固体,AgCl 沉淀的溶度积(Ksp)变小 | |
| D. | pH 相等的①CH3COONa ②NaHCO3溶液中,c(Na+)大小关系:②<① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1 | |
| B. | c(H+)=c(CH3COO-) | |
| C. | 加入少量CH3COONa固体后,醋酸的电离程度减小 | |
| D. | 与0.1 mol•L-1NaOH溶液等体积混合后所得溶液显中性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com