
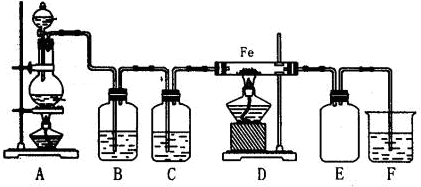
·ÖĪö £Ø1£©ŹµŃéŹŅÖʱøĀČĘųÓƵÄŌĮĻĪŖÅØŃĪĖįÓė¶žŃõ»ÆĆĢ£»
£Ø2£©¶žŃõ»ÆĆĢÓėÅØŃĪĖįŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³ÉĀČ»ÆĆĢ”¢ĀČĘųŗĶĖ®£»
£Ø3£©ÅØŃĪĖį¾ßÓŠ»Ó·¢ŠŌ£¬ÖʱøµÄĀČĘųÖŠŗ¬ÓŠĀČ»ÆĒā£¬ŅŖÖʱø“æ¾»µÄĀČĘųÓ¦³żČ„ĀČ»ÆĒā£¬½įŗĻĀČ»ÆĒā”¢ĀČĘųµÄČܽāŠŌŃ”ŌńŗĻŹŹµÄ³żŌÓ¼Į£»
£Ø4£©ĀČĘųÓėĒāŃõ»ÆÄĘ·“Ó¦£¬±»ĒāŃõ»ÆÄĘĪüŹÕ£¬ČŻŅ×·¢Éśµ¹Īü£¬×°ÖĆE×÷ÓĆŹĒ·ĄÖ¹µ¹ĪüµÄ·¢Éś£»
£Ø5£©ĀČĘųÓŠ¶¾£¬×°ÖĆFÖŠŹ¢ÓŠĒāŃõ»ÆÄĘÓėĀČĘų·“Ӧɜ³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘŗĶĖ®£®
½ā“š ½ā£ŗ£Ø1£©ŹµŃéŹŅÖʱøĀČĘųÓƵÄŌĮĻĪŖÅØŃĪĖįÓė¶žŃõ»ÆĆĢ£¬ĖłŅŌ·ÖŅŗĀ©¶·ÖŠĪŖÅØŃĪĖį£¬Ō²µ×ÉÕĘæÖŠŅ©Ę·ĪŖ¶žŃõ»ÆĆĢ£»
¹Ź“š°øĪŖ£ŗÅØŃĪĖį£»¶žŃõ»ÆĆĢ£»
£Ø2£©¶žŃõ»ÆĆĢÓėÅØŃĪĖįŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³ÉĀČ»ÆĆĢ”¢ĀČĘųŗĶĖ®£¬»Æѧ·½³ĢŹ½£ŗMnO2+4HCl£ØÅØ£© $\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2”ü+2H2O£»
¹Ź“š°øĪŖ£ŗMnO2+4HCl£ØÅØ£© $\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2”ü+2H2O£»
£Ø3£©ÅØŃĪĖį¾ßÓŠ»Ó·¢ŠŌ£¬ÖʱøµÄĀČĘųÖŠŗ¬ÓŠĀČ»ÆĒā£¬ŅŖÖʱø“æ¾»µÄĀČĘųÓ¦³żČ„ĀČ»ÆĒā£¬ĀČ»ÆĒāŅ×ČÜÓŚĖ®£¬¶ųĀČĘųŌŚ±„ŗĶŹ³ŃĪĖ®ÖŠČܽā¶Č²»“ó£¬ĖłŅŌæÉŅŌÓƱ„ŗĶŹ³ŃĪĖ®³żČ„ĀČĘųÖŠµÄĀČ»ÆĒā£¬
¹Ź“š°øĪŖ£ŗ±„ŗĶŹ³ŃĪĖ®£»
£Ø4£©ĀČĘųÓėĒāŃõ»ÆÄĘ·“Ó¦£¬±»ĒāŃõ»ÆÄĘĪüŹÕ£¬ČŻŅ×·¢Éśµ¹Īü£¬×°ÖĆE×÷ÓĆ×÷ĪŖ°²Č«Ę棬·ĄÖ¹µ¹ĪüµÄ·¢Éś£»
¹Ź“š°øĪŖ£ŗ°²Č«Ę棬·ĄÖ¹µ¹Īü£»
£Ø5£©ĀČĘųÓŠ¶¾£¬ĖłŅŌ×°ÖĆFµÄ×÷ÓĆŹĒĪ²ĘųĪüŹÕ£¬×°ÖĆFÖŠŹ¢ÓŠĒāŃõ»ÆÄĘÓėĀČĘų·“Ӧɜ³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘŗĶĖ®£¬»Æѧ·½³ĢŹ½£ŗ2NaOH+Cl2ØTNaCl+NaClO+H2O£»¹Ź“š°øĪŖ£ŗĪ²ĘųĪüŹÕ£»2NaOH+Cl2ØTNaCl+NaClO+H2O£®
µćĘĄ ±¾ĢāĶعżĀČ»ÆĢśµÄÖʱøĪŖŌŲĢ壬漲éĮĖĀČĘųµÄÖʱø”¢¾»»Æ”¢ŹÕ¼Æ”¢ŠŌÖŹµÄ¼ģŃéµČ£¬Ć÷Č·ĀČĘųÖʱøŌĄķŗĶĀČĘųµÄŠŌÖŹŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
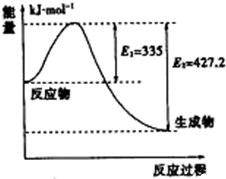 ÓÉ»ÆѧÄÜ×Ŗ±äµÄČČÄÜ»ņµēÄÜŹĒČĖĄąŹ¹ÓƵÄ×īÖ÷ŅŖµÄÄÜŌ“£®
ÓÉ»ÆѧÄÜ×Ŗ±äµÄČČÄÜ»ņµēÄÜŹĒČĖĄąŹ¹ÓƵÄ×īÖ÷ŅŖµÄÄÜŌ“£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
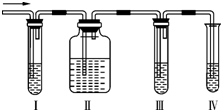 »ÆѧæĪĶāŠĖȤŠ”×éѧɜŌŚŹµŃéŹŅĄļÖĘČ”µÄŅŅĻ©ÖŠ³£»ģÓŠÉŁĮæµÄ¶žŃõ»ÆĮņ£¬ĄĻŹ¦Ęō·¢ĖūĆĒ²¢ÓÉĖūĆĒ×Ō¼ŗÉč¼ĘĮĖČēĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆŅŌČ·ČĻÉĻŹö»ģŗĻĘųĢåÖŠÓŠC2H4ŗĶSO2£®»Ų“šĻĀĮŠĪŹĢā£ŗ
»ÆѧæĪĶāŠĖȤŠ”×éѧɜŌŚŹµŃéŹŅĄļÖĘČ”µÄŅŅĻ©ÖŠ³£»ģÓŠÉŁĮæµÄ¶žŃõ»ÆĮņ£¬ĄĻŹ¦Ęō·¢ĖūĆĒ²¢ÓÉĖūĆĒ×Ō¼ŗÉč¼ĘĮĖČēĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆŅŌČ·ČĻÉĻŹö»ģŗĻĘųĢåÖŠÓŠC2H4ŗĶSO2£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
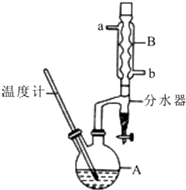 Õż¶”ĆŃ³£ÓĆ×÷ÓŠ»ś·“Ó¦µÄČܼĮ£®ŹµŃéŹŅÖʱøÕż¶”Ćѵķ“Ó¦ŗĶÖ÷ŅŖŹµŃé×°ÖĆČēĻĀ£ŗ2CH3CH2CH2CH2OH$?_{135”ę}^{ÅØĮņĖį}$£ØCH3CH2CH2CH2£©2O+H2O£¬·“Ó¦ĪļŗĶ²śĪļµÄĻą¹ŲŹż¾ŻČē±ķ£ŗ
Õż¶”ĆŃ³£ÓĆ×÷ÓŠ»ś·“Ó¦µÄČܼĮ£®ŹµŃéŹŅÖʱøÕż¶”Ćѵķ“Ó¦ŗĶÖ÷ŅŖŹµŃé×°ÖĆČēĻĀ£ŗ2CH3CH2CH2CH2OH$?_{135”ę}^{ÅØĮņĖį}$£ØCH3CH2CH2CH2£©2O+H2O£¬·“Ó¦ĪļŗĶ²śĪļµÄĻą¹ŲŹż¾ŻČē±ķ£ŗ| Ļą¶Ō·Ö×ÓÖŹĮæ | ·Šµć/”ę | ĆܶČ/£Øg/cm3£© | Ė®ÖŠµÄČܽāŠŌ | |
| Õż¶”“¼ | 74 | 117.2 | 0.8109 | Ī¢ČÜ |
| Õż¶”ĆŃ | 130 | 142.0 | 0.7704 | ¼øŗõ²»ČŻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| Ń”ÓĆŹŌ¼Į£ØĢīŠņŗÅ£© | ŹµŃéĻÖĻó | |
| ·½°ø1 | ||
| ·½°ø2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “ÓŗĻ³ÉĖž³öĄ“µÄ»ģŗĻĘųĢ壬ĘäÖŠNH3Ö»Õ¼15%£¬ĖłŅŌŗĻ³É°±¹¤³§µÄŠ§ĀŹ¶¼ŗܵĶ | |
| B£® | ÓÉÓŚ°±Ņ×Ņŗ»Æ£¬N2”¢H2ŹĒŃ»·Ź¹ÓĆ£¬ĖłŅŌ×ÜĢåĄ“Ėµ°±µÄ²śĀŹŗÜøß | |
| C£® | ŗĻ³É°±¹¤ŅµµÄ·“Ó¦ĪĀ¶ČæŲÖĘŌŚ500”ę×óÓŅ£¬ÄæµÄŹĒŹ¹»ÆŃ§Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ | |
| D£® | ŗĻ³É°±¹¤³§²ÉÓƵÄŃ¹ĒæŹĒ2”Į107”«5”Į107Pa£¬ŅņĪŖŌŚøĆŃ¹ĒæĻĀĢś“„Ć½µÄ»īŠŌ×ī“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ōö“ó·“Ó¦ĢåĻµµÄŃ¹Ē棬·“Ó¦ĖŁĀŹŌö“ó | |
| B£® | ¼ÓČėĢ¼·Ū£¬Ę½ŗāĻņÓŅŅĘ¶Æ£¬ŌŅņŹĒĢ¼ÓėO2·“Ó¦£¬½µµĶĮĖÉś³ÉĪļµÄÅضČĒŅ·Å³öČČĮæ | |
| C£® | µē½āČŪČŚµÄAl2O3ŗĶAlCl3¾łÄܵƵ½µ„ÖŹĀĮ | |
| D£® | ÉżøßĪĀ¶Č£¬·“Ó¦µÄĘ½ŗā³£Źż½«Ōö“ó |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com