
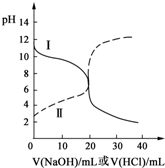
 25℃时取浓度均为0.1000mol•L-1的CH3COOH(aq)和氨水各20mL,分别用0.1000mol•L-1NaOH(aq)、0.1000mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时取浓度均为0.1000mol•L-1的CH3COOH(aq)和氨水各20mL,分别用0.1000mol•L-1NaOH(aq)、0.1000mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A. | 曲线Ⅰ:滴加溶液到10.00mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| B. | 曲线Ⅱ:滴加溶液到10.00mL时:c(CH3COO-)-c(CH3COOH)=2[c(OH-)-c(H+)] | |
| C. | 曲线Ⅱ:滴加溶液在10.00mL~20.00mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) | |
| D. | 曲线Ⅰ:滴加溶液到20.00mL时,c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
分析 曲线I开始时pH>7,滴定过程中pH减小,是用盐酸滴定氨水,曲线Ⅱ开始时pH<7,滴定过程中pH增大,是用氢氧化钠滴定醋酸.
A.曲线Ⅰ是用盐酸滴定氨水;
B.曲线Ⅱ中滴加溶液到10.00mL时,得到等浓度的CH3COOH、CH3COONa混合溶液,结合微粒守恒、电荷守恒判断;
C.曲线Ⅱ是用氢氧化钠滴定醋酸;
D.曲线I中滴加溶液到20.00mL时,得到NH4Cl溶液,溶液中铵根离子水解,溶液呈酸性.
解答 解:曲线I开始时pH>7,滴定过程中pH减小,是用盐酸滴定氨水,曲线Ⅱ开始时pH<7,滴定过程中pH增大,是用氢氧化钠滴定醋酸.
A.曲线Ⅰ是用盐酸滴定氨水,故A错误;
B.曲线Ⅱ中滴加溶液到10.00mL时,得到等浓度的CH3COOH、CH3COONa混合溶液,根据物料守恒可得:c(CH3COOH)+c(CH3COO-)=2c(Na+),根据电荷守恒:c(CH3COO-)+c(OH-)=c(Na+)+c(H+),联立可得:2c(OH-)-2c(H+)=c(CH3COOH)-c(CH3COO-),故B错误;
C.曲线Ⅱ是用氢氧化钠滴定醋酸,故C错误;
D.曲线I中滴加溶液到20.00mL时,得到NH4Cl溶液,溶液中铵根离子水解,溶液呈酸性,则溶液中c(Cl-)>c(NH4+)>c(H+)>c(OH-),故D正确.
故选:D.
点评 本题考查中和滴定、离子浓度大小比较,关键是根据滴定曲线判断相互滴定的物质,注意掌握溶液酸碱性与溶液pH的关系,能够根据电荷守恒、物料守恒及盐的水解判断溶液中离子浓度大小.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.5mol/L KCl溶液 | B. | 自来水 | ||
| C. | 0.5mol/L盐酸 | D. | 0.5mol/L醋酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁杵成针 | B. | 抱薪救火 | C. | 闭门造车 | D. | 刻舟求剑 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
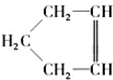 ,可简写为
,可简写为 ,降冰片烯的分子结构可表示为
,降冰片烯的分子结构可表示为 .
. .(任选一种)
.(任选一种)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
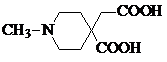 .
.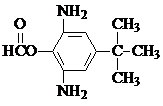 或
或 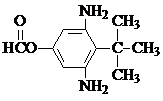 .
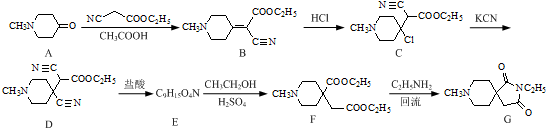
.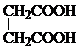 和CH3CH2Cl为原料制备
和CH3CH2Cl为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由C(s,石墨)═C(s,金钢石)△H>0可知,金刚石比石墨稳定 | |
| B. | CO(g)燃烧热是283.0 kJ•mol-1,则2CO2(g)═2CO(g)+O2(g)△H=+566.0kJ•mol-1 | |
| C. | CH4(g)+2O2(g)═CO2+2H2O(I)△H<0,该反应的化学能可以转化为电能 | |
| D. | 已知C(s)+O2(g)═CO2(g)△H1,C(s)+$\frac{1}{2}$O2(g)═CO(g)△H2,则)△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨、液氯、干冰、碘化银均为化合物 | |
| B. | 明矾、小苏打、醋酸、次氯酸均为电解质 | |
| C. | 碘酒、牛奶、豆浆、漂白粉均为胶体 | |
| D. | Na2O2、Na2CO3、Na2SiO3、KNO3均为盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com