
【题目】(1)已知:2Fe2O3(s)+3C(s)=3CO2(g)+4Fe(s) ΔH1=+234.1 kJ·mol-1①
C(s)+O2(g=CO2(g) ΔH2=-393.5 kJ·mol-1②
则Fe和O2反应生成Fe2O3的热化学反应方程式为_______________________________。
(2)已知H2A在水中存在以下平衡:H2A=H++HA-,HA-![]() H++A2-。
H++A2-。
①常温下NaHA溶液的pH________(填序号),原因是____________________________。
A.大于7 B.小于7 C.等于7 D.无法确定
②已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s)![]() Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有______________________。
Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有______________________。
A.升高温度 B.降低温度 C.加入NH4Cl晶体 D.加入Na2A固体
(3)实验室中有一未知浓度的稀盐酸,某学生用0.10 mol·L-1 NaOH标准溶液进行测定盐酸的浓度的实验。取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验编号 | NaOH溶液的浓度(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸的体积(mL) |
1 | 0.10 | 22.65 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.93 | 20.00 |
请完成下列填空:
①滴定达到终点的标志是_____________________________________________。
②根据上述数据,可计算出该盐酸的浓度约为_____________________(保留两位有效数字)。
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________(填字母序号)。
A.滴定终点读数时俯视
B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥
D.称量NaOH固体中混有Na2CO3固体
E.碱式滴定管尖嘴部分有气泡,滴定后消失
【答案】 4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1414.6 kJ·mol-1 B NaHA只能发生电离,不能发生水解 BD 最后一滴NaOH溶液滴入,溶液由无色恰好变成粉红色且半分钟内不褪色 0.11 mol·L-1 DE
【解析】(1)反应①×(-1)+反应②×3得到:4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1414.6 kJ·mol-1。
(2)①根据题目已知,H2A的第一步电离不可逆,第二步电离可逆,所以HA-在溶液中只存在电离不存在水解,所以NaHA的溶液一定显酸性,pH小于7。
②要使该溶液中Ca2+浓度变小,应该采取措施使平衡逆向移动。反应吸热,升高温度,平衡正向移动,选项A错误。降低温度,平衡逆向移动,选项B正确。加入氯化铵固体,铵根离子的水解对A2-的水解产生促进作用,所以A2-的浓度减小,平衡正向移动,选项C错误。加入Na2A固体,A2-的浓度增大,平衡逆向移动,选项D正确。所以答案为BD。
(3)①指示剂为酚酞,滴定终点时,溶液由无色转化为粉红色,所以标志为:最后一滴NaOH溶液滴入,溶液由无色恰好变成粉红色且半分钟内不褪色。
②盐酸的浓度为![]() 。
。
③滴定终点的时候俯视,即向下看,所以会将滴加的氢氧化钠溶液体积读小,结果会偏低,选项A错误。酸式滴定管使用前,水洗后未用待测盐酸润洗,会使滴定管内盐酸的浓度减小,自然会使滴定结果变小,选项B错误。锥形瓶水洗之后,不需要干燥,所以是无影响,选项C错误。称量NaOH固体中混有Na2CO3固体,所以导致氢氧化钠标准溶液的浓度变小,最后使加入的氢氧化钠溶液的体积增加,导致滴定结果增大,选项D正确。碱式滴定管尖嘴部分有气泡,滴定后消失,导致加入的氢氧化钠溶液的体积增加(增加了一个气泡的体积),最终滴定结果增大,选项E正确。


科目:高中化学 来源: 题型:
【题目】小麦种子萌发时产生淀粉酶,将淀粉水解为麦芽糖、葡萄糖等。小麦种子萌发的最适温度为30℃左右。取适量小麦种子在20℃和30℃培养箱中培养4天后,做如下处理:在3支试管中加入等量斐林试剂并加热至50℃左右,摇匀后观察试管中的颜色。结果是( )

A.甲呈蓝色,乙呈砖红色,丙呈无色
B.甲呈无色,乙呈砖红色,丙呈蓝色
C.甲、乙皆呈蓝色,丙呈砖红色
D.甲呈浅砖红色,乙呈砖红色,丙呈蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚氮化硫(SN)x和K3C60是两种不同类型的超导材料。回答下列问题:
(1)在基态K原子中,能量最低的空轨道的符号是_____________。
(2)S、N、K三种元素的第一电离能由大到小的顺序是____________。
(3)(SN)x具有类似黄铜的金属光泽和导电性,其结构如下图:
![]()
以S2Cl2为原料可制取(SN)x:S2Cl2→…S4N4 ![]() S2N2
S2N2 ![]() (SN)x
(SN)x
①(SN)x中N原子的杂化方式是_________;(SN)x的晶体类型是______;
②S2Cl2的结构式为________;
③Ag元素位于周期表第5周期、IB族,基态Ag原子的价电子排布式为__________。
(4)K3C60是由足球烯(C60)与金属钾反应生成的盐。
①在K3C60晶胞中,C603-堆积方式为面心立方结构,每个晶胞中形成4个八面体空隙和8个四面体空隙,K+填充在空隙中。晶胞中被K+占据的空隙百分比为___________。
②C60与金刚石互为同素异形休,比较两者的熔沸点并说明理由____________。
③C60的结构是一种多面体,如图。多面体的顶点数、面数和棱边数的关系遵循欧拉定律:顶点数+面数-棱边数=2。C60分子中所含的五边形和六边形的个数分别为_____、______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2通入下列溶液中,溶液褪色或变浅,说明SO2具有漂白作用的组合是( )
①KMnO4(H+ , aq) ②溴水 ③碘水 ④氯水 ⑤Fe3+(aq)
A.①⑤
B.②③
C.全部
D.都不是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向25mL0.1molL-1NaOH溶液中逐滴滴加0.2molL-1的一元酸HX溶液,pH的变化曲线如下图所示(溶液混合时体积的变化忽略不计).下列说法正确的是( )
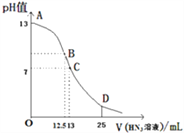
A. 在B点,离子浓度大小为c(OH-)>c(H+)>c(Na+)>c(X-)
B. D点的溶液中c(H+)+c(HX)=c(X-)+c(OH-)
C. HX是弱酸,常温下其电离常数Ka=2.5×10-6
D. D点的溶液中有c(HX)-2c(H+)=2c(OH-)+c(X-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 水的离子积常数KW只与温度有关,但若外加酸、碱会抑制水的电离,若外加盐则可能促进水的电离或不影响水的电离。
B. Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关。
C. 常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使溶液的pH减小,c(NH![]() )/c(NH3·H2O)的值增大,故使NH3·H2O的Kb会减小。
)/c(NH3·H2O)的值增大,故使NH3·H2O的Kb会减小。
D. 室温下,CH3COOH的Ka=1.7×10-5,NH3·H2O的Kb=1.7×10-5,CH3COOH溶液中的c(H+)与NH3·H2O中的c(OH-)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0 L恒容密闭容器中充入2.0 mol X,反应X(g) ![]() Y(g)+Z(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
Y(g)+Z(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(Y)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
下列说法不正确的是
A. 反应在前250 s的平均速率为v(Y)=0.000 8 mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(Y)=0.21 mol·L-1,则反应的ΔH>0
C. 相同温度下,起始时向容器中充入4.0 mol Y、4.0 mol Z,达到平衡时,则此反应的化学平衡常数为1/20
D. 相同温度下,若起始时向容器中充入2.0 mol X、0.40 mol Y和0.80 mol Z,则达到平衡前v(正)>v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,CO(g)+H2O(g)CO2(g)+H2(g)的平衡常数K=1.该温度下在体积均为1L的甲、乙两个恒容密闭容器中,投入CO(g)和H2O(g)的起始浓度及5min时的浓度如表所示.下列判断不正确的是( )
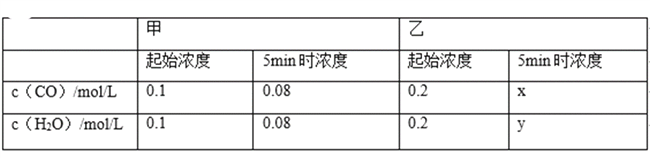
A. x=y=0.16
B. 反应开始时,乙中反应速率比甲快
C. 甲中0~5min的平均反应速率:v(CO)=0.004 mol/(Lmin)
D. 平衡时,乙中H2O的转化率是50%,c(CO)是甲中的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.5 mol CH4的质量为________g,约含有______个H,在标准状况下的体积为_______L。
(2)相同质量的CO和CO2,它们所含的原子数之比为_______,在同温同压下,它们的密度之比为______;等物质的量的CO和CO2的混合气体的密度是相同条件下氢气密度的__________倍。
(3)12.4 g Na2R含Na+0.4 mol,则R的相对原子质量为_____________。
(4)已知16 g肼(N2H4)含有的电子数为b,则阿伏加德罗常数为______________。(用含b的式子表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com