
| A. | 用A表示的反应速率是0.4 mol/(L•min) | |
| B. | 用B、C、D分别表示反应的速率,其比值是3:2:1 | |
| C. | 在2min末的反应速率用B表示是0.3 mol/(L•min) | |
| D. | 在这2min内用B和C表示的速率的值都是逐渐增大的 |
分析 经2min,B的浓度减少0.6mol/L,v(B)=$\frac{0.6mol/L}{2min}$=0.3mol•(L•min)-1,结合反应速率之比等于化学计量数之比来解答.
解答 解:经2min,B的浓度减少0.6mol/L,v(B)=$\frac{0.6mol/L}{2min}$=0.3mol•(L•min)-1,
A.A物质为纯固体,不能表示反应速率,故A错误;
B.反应速率之比等于化学计量数之比,则分别用B、C、D表示的反应速率其比值是3:2:1,故B正确;
C.反应速率为平均速率,则在2min内的平均反应速率,用B表示是0.3 mol•(L•min)-1,故C错误;
D.B为反应物,C为生成物,则在这2min内用B和C表示的反应速率的值分别为逐渐减小、逐渐增大,故D错误;
故选B.
点评 本题考查化学反应速率的计算及与化学计量数的关系,明确计算公式及反应速率为平均速率即可解答,注意选项A为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
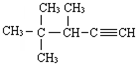 的系统名称为( )
的系统名称为( )| A. | 2,2,3一三甲基一1-戊炔 | B. | 3,4,4一三甲基一l一戊炔 | ||
| C. | 3,4,4一三甲基-2一戊炔 | D. | 2,2,3一三甲基一4一戊炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该燃料绿色环保,在燃烧过程中不会造成任何环境污染 | |
| B. | 该反应中N2O4是氧化剂,偏二甲肼是还原剂 | |
| C. | N2既是氧化产物又是还原产物,CO2既不是氧化产物也不是还原产物 | |
| D. | 每有0.6 mol N2生成,转移电子数目为2.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
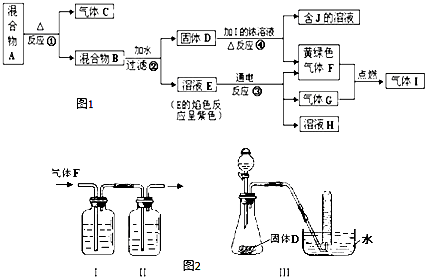
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
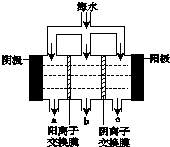 《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.
《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ②④⑤ | C. | ①③④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、H+、SO42-、OH- | B. | Ca2+、Na+、NO3-、CO32- | ||
| C. | Na+、H+、CO32-、Cl- | D. | Na+、Cl-、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com