
| A. | 达到平衡时,再充入1molX,该反应的△H变大 | |
| B. | 用Y表示4min内的反应速率为0.1mol/(L•min) | |
| C. | 再向容器中充入1molZ,达到新平衡,n(X):n(Y)=2:1 | |
| D. | 4min后,若升高温度,平衡将向逆反应方向移动,平衡常数K减小 |
分析 A.热化学方程式中的焓变与化学计量数有关,与参加反应的反应物的物质的量无关;
B.根据v=$\frac{△c}{△t}$计算v(X),再利用速率之比等于化学计量数之比计算v(Y);
C.原平衡时X与Y的转化率相等,说明X、Y的起始物质的量之比等于化学计量数之比2:1,再向容器中充入1molZ,平衡向逆反应方向移动,反应过程中X、Y的物质的量之比为2:1,达新平衡时X、Y的物质的量之比不变;
D.升高温度,平衡向逆反应方向移动.
解答 解:A.热化学方程式中的焓变与化学计量数有关,与参加反应的反应物的物质的量无关,再充入1molX,平衡向正反应方向移动,但应热化学方程式中的焓变保持不变,故A错误;
B.v(X)=$\frac{\frac{2mol}{2L}-0.2mol/L}{4min}$=0.2mol•L-1•min-1,速率之比等于化学计量数之比,则v(Y)=$\frac{1}{2}$v(X)=0.1mol•L-1•min-1,故B正确;
C.原平衡时X与Y的转化率相等,说明X、Y的起始物质的量之比等于化学计量数之比2:1,再向容器中充入1molZ,平衡向逆反应方向移动,反应过程中X、Y的物质的量之比为2:1,达新平衡时X、Y的物质的量之比不变为2:1,故达到新平衡,c(X):c(Y)=2:1,故C正确;
D.该反应正反应是放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,故D正确;
故选:A.
点评 本题考查化学平衡计算、化学平衡常数等,难度中等,注意反应物的起始物质的量之比等于化学计量数之比则转化率相等.


科目:高中化学 来源: 题型:选择题
| A. | 维生素C与“金施尔康”都是氧化剂 | |
| B. | 维生素C与“金施尔康”都是还原剂 | |
| C. | 维生素C是氧化剂,“金施尔康”是还原剂 | |
| D. | 维生素C是还原剂,“金施尔康”是氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2中阴、阳离子的个数比为1:1 | |
| B. | Na202比Na2O稳定,保存时可直接露置于空气中 | |
| C. | Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等 | |
| D. | Na2O2分别与水及CO2反应产生相同量的O2时,转移电子的物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A和B的平衡浓度之比为5:3 | B. | A和B的平衡浓度之比为2:3 | ||
| C. | x=1 | D. | x:y=2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
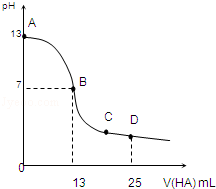 常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:
常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com