
��������������Ϣ��Ȼ��ش��й����⣺
����һ����PbO+C Pb+CO������PbO+CO
Pb+CO������PbO+CO Pb+CO2����[Cu��NH3��2]Ac+CO+NH3[Cu��NH3��3]Ac•CO��
Pb+CO2����[Cu��NH3��2]Ac+CO+NH3[Cu��NH3��3]Ac•CO��
���϶���NH4NO2���ȶ������ȷֽ����������
ʵ��Ŀ�ģ�̽��PbO�к��е���Ԫ�أ�
��1��д��װ�ü������ɵ����Ļ�ѧ����ʽ������
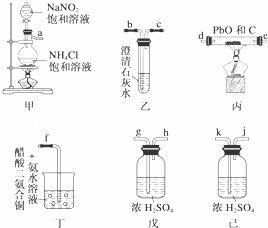
��2��ʵ����ʹ�õ�װ������ͼ��ʾ���밴�յ������������Ӹ����������������ӿڴ���ĸ��ţ�����a����������������������������
��3����ʼʱ��װ�����еij���ʯ��ˮ��ֻ�����ݣ�û�а�ɫ���dz��֣��������������ԭ����������
��4���ձ��д��������ͭ[Cu��NH3��2]Ac������������
��5����ͬѧ��Ϊ��ʵ���ø���Ŀ������Դ������ĵ���������Ϊ�����뷨�Ƿ���У�˵�����ɣ�������
| ̽�����ʵ���ɻ�������ʵĺ����� | |
| ר�⣺ | ʵ��̽�������ݴ����⣮ |
| ������ | ��ʵ���Ŀ���DzⶨPbO�к��е���Ԫ�أ��������ڼ��ȵ�������ʹ̼��PbO��Ӧ��Ȼ���ó���ʯ��ˮ����������Ƿ���CO2���ڣ� ��1��װ�ü��з���������Ӧ��һ�����Ȼ�����������Ƶĸ��ֽⷴӦ������������泥���һ�����ڼ���������������立ֽ���������� ��2������ʵ�����������Ʊ�������Ȼ�������ڼ��ȵ�������C��PbO��Ӧ���ó���ʯ��ˮ������������̼������ȥ��������е��к�����CO�� ��3��������̼ʹ����ʯ��ˮ����ǣ���һ����̼����ʹ����ʯ��ˮ����ǣ� ��4������֪�Ļ�ѧ����ʽ��֪���������ͭ�ܹ�����CO�����������Ƿ�ֹCO�ݳ���Ⱦ������ ��5�����ø���Ŀ����������ĵ�����������е�������̼��Ӧ���ɶ�����̼������˵��������̼�е�������PbO�� |
| ��� | �⣺��ʵ���Ŀ���DzⶨPbO�к��е���Ԫ�أ��������ڼ��ȵ�������ʹ̼��PbO��Ӧ��Ȼ���ó���ʯ��ˮ����������Ƿ���CO2���ڣ� ��1���Ȼ�����������Ƶĸ��ֽⷴӦ������������立�Ӧ����ʽΪNH4Cl+NaNO2 ��2������ʵ�����������Ʊ�����������װ�üף��Ƚ�a��Ȼ����Ũ��������g��h����k��j�������ڼ��ȵ�������ͨ��װ�ñ�C��PbO��Ӧ���ʽ�d��e����e��d�����ó���ʯ��ˮ������������̼������ȥ��������е��к�����CO����b��c���ʴ�Ϊ��g��h����k��j����d��e����e��d����b��c�� ��3��PbO+C ��4�����ݷ�Ӧ��[Cu��NH3��2]Ac+CO+NH3=[Cu��NH3��3]Ac•CO��֪���������ͭ�ܹ�����CO�����������Ƿ�ֹCO�ݳ���Ⱦ�������ʴ�Ϊ������CO���壬��ֹCO�ݳ���Ⱦ������ ��5����Ӧ��ϵ��ͨ�����ĵ�����Ŀ���Ƿ�ֹ�����е�����Ӱ��ʵ���������ø���Ŀ����������ĵ�����������е�������̼��Ӧ���ɶ�����̼������˵��������̼�е�������PbO���ʴ�Ϊ�������У���Ϊ�����е�������̼��ӦҲ����������̼����ȷ��������̼�е�������������PbO���ǿ����� |
| ������ | ���⿼�������ʵĺ����IJ�������Ŀ�ѶȽϴ�ע�����ʵ�鷽����ʱ���������ԡ������ԣ�����Ĺؼ��Ǹ��������ṩ����Ϣ������е�֪ʶ���з����������ۺ���ǿ��ּ������ѧ��������û���֪ʶ���ʵ�����������������������ѧ���������������ͷ�ɢ˼ά������ |
��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij���������л������ֻ��̼���⡢������Ԫ�أ���Է�������Ϊ58����ȫȼ
��ʱ���������ʵ�����CO2��H2O�������ܵĽṹ���У������������칹��
A��4�� B��5�� C��6�� D��7��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
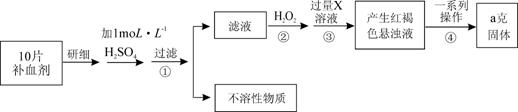
ijƷ������Ƭ��Ѫ������ȥ���º��Ե�����ɫ����Ҫ�ɷ������������������������Ļ����ij�о���ѧϰС��Ϊ�ⶨ�ò�Ѫ�������������ĺ�������������̽����
 |
��ش��������⣺
��1��ʵ��ʱ��18.4 mol��L-1��Ũ���ᣬ����100 mL 1 mol��L-1 H2SO4��Һ������Ũ��������Ϊ ������������ȷ��С�����һλ��
��2�����в����У�����ƿ���߱��Ĺ����� (�����)��
A������һ�����ȷŨ�ȵı���Һ B������������Һ
C�������ܽ�������� D��������������Ͳ��ȡһ�������Һ��
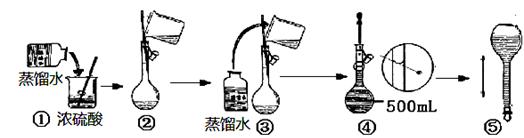 ��3�����������ƹ���ʾ��ͼ�У��д�����ǣ���д��ţ� ��
��3�����������ƹ���ʾ��ͼ�У��д�����ǣ���д��ţ� ��
 | |||||
| |||||
|
��4������˵����ȷ��
A��ϴ���ձ�2~3�Σ�����ϴ��Һ��������ƿ�Լ������
B��ijͬѧ��Ũ����ϡ�ͺ�δ��ȴ�����±㽫��Һת��������ƿ��������ҺŨ�Ȼ�ƫ��
C������ʱ���ӹ۲�, ������ҺŨ�Ȼ�ƫ��
D������ƿʹ��ǰ��Ҫ����Ƿ�©Һ�����������������ƿ�м�����ˮ�����ò�©Һ����
��1������ڼ������H2O2��Ŀ�ģ� ��
��2���Ӻ��ɫ������Һ�����ij����������������Ļ�������Ϊ��
a. ��b. ϴ�ӣ�c. ���գ�d. ��ȴ
��3�����Ƶù��������Ϊag����ÿƬ��Ѫ���к���������������Ϊ ��
����֪���岻�ܺܺõ���������Fe3+����ѧ�о��������ú����������IJ�Ѫ��ʱ��ͬʱ����ά����C����������Ԫ�ص����ա��Է���ά����C����һ�����е������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������KSCN��SCN���ǡ���±���ӡ������������������ƣ���Һ�������Եĺ���Fe3+����Һ�У���Һ���Ѫ��ɫ�����ú�ɫ��Һ��Ϊ���ݣ���һ���м�������KMnO4��Һ����ɫ��ȥ��������һ����ͨ��SO2����ɫҲ��ȥ������˵������ȷ���ǣ�������
| �� | A�� | �ٺ�ɫ��ȥ��ԭ�������KMnO4��SCN��������ʹ[Fe��SCN��]2+��ʧ |
| �� | B�� | [Fe��SCN��]2+��Fe3+��SCN���������� |
| �� | C�� | �ں�ɫ��ȥ��ԭ����SO2���л�ԭ�� |
| �� | D�� | SCN�����ʵ������¿ɱ���ԭΪ��SCN��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ����������ͨ��30mLŨ��Ϊ10.00mol/L����������Ũ��Һ�У���������ʱ�����Һ���γ�NaCl��NaClO��NaClO3������ϵ�������ж���ȷ���ǣ�������
| �� | A�� | ��NaOH��Ӧ������һ��Ϊ0.3 mol |
| �� | B�� | n��Na+����n��Cl��������Ϊ7��3 |
| �� | C�� | ����Ӧ��ת�Ƶĵ���Ϊn mol����0.15��n��0.25 |
| �� | D�� | n��NaCl����n��NaClO����n��NaClO3������Ϊ11��2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij����һԪȩ����������Ӧʱ��������21.6g����������ȩ��ȫȼ�տ��Բ���8.96LCO2����״������
���ȩΪ �� ��
A����ȩ  B����ȩ C����ȩ D����ȩ
B����ȩ C����ȩ D����ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ���Թܢ����ȼ���3mL 95�����Ҵ��� ����ҡ���»�������2mLŨ���ᣬ���ҡ�ȣ���ȴ���ټ���2mL��ˮ���ᣬ�ò�������ֽ�����Թ̶ܹ�������̨�ϣ����Թܢ��м���5ml ���͵�̼������Һ����ͼ���Ӻ�װ�ã��þƾ��ƶ��Թܢ�С�����3��5min���ô����ȣ����۲쵽�Թܢ�������������ʱֹͣ���ȡ��Իش�
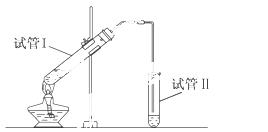
��1���Թܢ��еĵ��ܲ�����Һ���µ�ԭ���� ��
��2����Ӧ��Ϻ����Թܢ۲쵽�Թܢ��е������� ��
��3���Թܢ��м���Ũ����������� ��
��4����ʵ�鷴Ӧ��ʼʱ��С����ȵ�ԭ���� ________������֪���������ķе�Ϊ77�棻�Ҵ��ķе�Ϊ78.5�棻����ķе�Ϊ117.9�棩
________������֪���������ķе�Ϊ77�棻�Ҵ��ķе�Ϊ78.5�棻����ķе�Ϊ117.9�棩
��5���Թܢ��б���Na2 CO3��������
CO3��������
��6��д���Թܢ��з�����Ӧ�Ļ�ѧ����ʽ 
�÷�Ӧ�ķ�Ӧ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���г�ȥ���ʵķ�����ȷ���� (����)
A����ȥCO2�л��е�CO���ó���ʯ��ˮϴ��
B����ȥBaCO3�����л��е�BaSO4���ӹ���������ˡ�ϴ��
C����ȥFeCl2��Һ�л��е�FeCl3������������ۣ�����
D����ȥCu���л��е�CuO��������ϡ������ˡ�ϴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������������ȷ����
A����ȼ�Լ���ǿ�������Լ��ֿ����ò�Զ���Դ
B����ʪ��ĺ�ɫʯ����ֽ���鰱��
C����50mL��Ͳ������0.1000mol·L-1̼������Һ
D���������Ż�ʱ����ϸɳ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com