
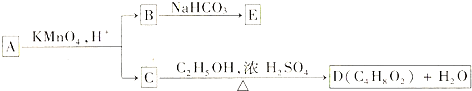
���� ������������Ϊ0.186���ٶ�A����Է�������Ϊ90����N��O��=$\frac{90��0.186}{16}$=1.0463����������ԭ�Ӹ���Ϊ1����A����Է�������Ϊ��$\frac{16}{0.186}$=86�������෨��$\frac{86-16}{12}$=5��10������A�÷���ʽΪC5H10O�����C+C2H5OH$��_{��}^{Ũ����}$C4H8O2+H2O��֪��CΪCH3COOH��DΪCH3COOC2H5������B��NaHCO3��Һ��ȫ��Ӧ�������ʵ���֮��Ϊ1��2������B�к���2��-COOH��B�к���3��Cԭ�ӣ�����֪B�к���2��-COOH����B�л�����һ��CH2������B�Ľṹ��ʽΪHOOCCH2COOH���л���EΪNaOOCCH2COONa��A��������������÷ų�������˵��A�к��еĹ�����Ϊ-OH����ʹ������Ȼ�̼��Һ��ɫ��˵��A�к���C=C����AΪֱ������������Ŀ��Ϣ��B��C�ṹ���ɵ�A�Ľṹ��ʽΪ��HOCH2CH2CH=CHCH3���ݴ˽��
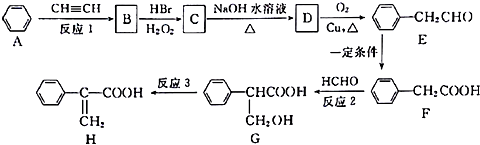
��� �⣺��1��������������Ϊ0.186���ٶ�A����Է�������Ϊ90����N��O��=$\frac{90��0.186}{16}$=1.0463����������ԭ�Ӹ���Ϊ1����A����Է�������Ϊ��$\frac{16}{0.186}$=86�������෨��$\frac{86-16}{12}$=5��10������A�÷���ʽΪC5H10O��
�ʴ�Ϊ��C5H10O��
��2�����C+C2H5OH$��_{��}^{Ũ����}$C4H8O2+H2O��֪��CΪCH3COOH��DΪCH3COOC2H5������B��NaHCO3��Һ��ȫ��Ӧ�������ʵ���֮��Ϊ1��2������B�к���2��-COOH��B�к���3��Cԭ�ӣ�����֪B�к���2��-COOH����B�л�����һ��CH2������B�Ľṹ��ʽΪHOOCCH2COOH��B��������C2H5OH��Ӧ�Ļ�ѧ����ʽΪ��HOOCCH2COOH+2C2H5OH$��_{��}^{Ũ����}$C2H5OOCCH2COOC2H5+2H2O��
�ʴ�Ϊ��HOOCCH2COOH+2C2H5OH$��_{��}^{Ũ����}$C2H5OOCCH2COOC2H5+2H2O��
��3��A��������������÷ų�������˵��A�к��еĹ�����Ϊ-OH����ʹ������Ȼ�̼��Һ��ɫ��˵��A�к���C=C����AΪֱ������������Ŀ��Ϣ��B��C�ṹ���ɵ�A�Ľṹ��ʽΪ��HOCH2CH2CH=CHCH3��
�ʴ�Ϊ��HOCH2CH2CH=CHCH3��
��4��DΪCH3COOC2H5����ͬ���칹������NaHCO3��Һ��Ӧ�ų�CO2��˵��Ϊ���ᣬ��ṹ��ʽΪ��CH3CH2CH2COOH��CH3CH��CH3��COOH��
�ʴ�Ϊ��2��
���� ���⿼���л�����ƶϣ��ؼ��Ǽ���ȷ��A�ķ���ʽ���ٽ����Ŀ��Ϣ����Ӧ������D�ķ���ʽ�����ƶϣ����ؿ���ѧ�����������������Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
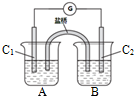 ��֪�飨As��Ԫ�ص�ԭ�ӽṹʾ��ͼΪ
��֪�飨As��Ԫ�ص�ԭ�ӽṹʾ��ͼΪ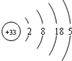
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
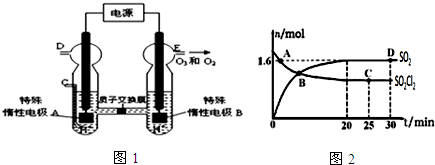
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� +NaOH $��_{��}^{ˮ}$
+NaOH $��_{��}^{ˮ}$ +NaBr��
+NaBr�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1molNa2O2�����������ӵĸ���Ϊ2NA | |
| B�� | ��״���£�2.24L�������ķ�������Ϊ0.1NA | |
| C�� | 32gO2��32g O3����������ԭ��������Ϊ2NA | |
| D�� | 6.4gͭ�������Ũ������ȫ��Ӧת�Ƶĵ�������0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | XQ2W�����ڳ����³���̬�������е��ĸ�ԭ����ͬһƽ���� | |
| B�� | Z��W�γɵ��������ӻ����������������Ӹ����Ⱦ�Ϊ2��1 | |
| C�� | X��W��Ԫ�طֱ��QԪ�ػ��ϣ����γɵ�������ͬ�����ֻ����� | |
| D�� | ��Ӧ�����Ӱ뾶��С��ϵΪ��Y��W��Z |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=1����Һ�У�Na+��NH4+��SO42-��ClO- | |
| B�� | KW/c��H+��=0.1 mol•L-1����Һ�У�Na+��K+��MnO4-��HCO3- | |
| C�� | 0.1 mol•L-1��Na2SO3��Һ�У�K+��H+��SO42-��NO3- | |
| D�� | ����������Һ�У�Fe3+��Na+��Cl-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ԣ�HClO4��H2SO4��H3AsO4��H3PO4 | |
| B�� | ���ԣ�Ca��OH��2��Mg��OH��2��Al��OH��3 | |
| C�� | ���������û������������Cs��Rb��K��Ca | |
| D�� | �����ԣ�F2��Cl2��S |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com