
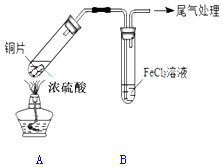
 某校化学兴趣小组用如图装置进行SO2与FeCl3溶液的反应
某校化学兴趣小组用如图装置进行SO2与FeCl3溶液的反应分析 加热条件下,铜和浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫通入氯化铁溶液中,溶液由黄色变为浅绿色,说明二氧化硫和氯化铁发生氧化还原反应,以此解答该题.
解答 解:(1)装置A利用铜与浓硫酸加热反应生成硫酸铜、二氧化硫和水来制备二氧化硫,方程式为:Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)B中溶液由黄色变为浅绿色,说明二氧化硫和氯化铁发生氧化还原反应,故答案为:B中氯化铁溶液颜色变化;由浅黄色变为浅绿色;
(3)氯化铁具有氧化性,除此之外还可与碱反应生成红褐色氢氧化铁沉淀,发生Fe3++3OH-=Fe(OH)3↓,可取少量溶液滴加氢氧化钠溶液,观察生成红褐色沉淀,
故答案为:Fe3++3OH-=Fe(OH)3↓;取少量溶液滴加氢氧化钠溶液,观察生成红褐色沉淀.
点评 本题考查性质实验方案的设计,为高频考点,把握发生的氧化还原反应原理及反应中元素的化合价变化为解答的关键,侧重分析能力、实验能力及归纳能力的考查,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,17g NH3所含的电子数是 10NA | |
| B. | 常温常压下,22.4L氧气含氧原子数为2NA | |
| C. | 0.5 mol/L K2SO4溶液中含有NA个K+离子 | |
| D. | 2.3g金属钠与氧气反应全部生成Na2O时失去的电子数是0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaHCO3溶液中滴加澄清石灰水,不会产生沉淀 | |
| B. | 等质量NaHCO3和Na2CO3分别与足量盐酸反应,生成的CO2在同温同压下体积相同 | |
| C. | 向Na2CO3溶液中缓慢通入等物质的量的HCl,生成的CO2与原Na2CO3的物质的量之比为1:2 | |
| D. | 向Na2CO3饱和溶液中通入CO2,有晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在容量瓶中定容时,俯视刻度线 | |
| B. | 用量筒量取浓盐酸时,俯视刻度线 | |
| C. | 转移溶液后,未洗涤烧杯和玻璃棒就直接定容 | |
| D. | 定容后把容量瓶倒置摇匀,发现液面低于刻度线又加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0.1mol•L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 在0.1mol•L-1Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H2CO3)+c(H+) | |
| C. | 向0.2 mol•L-1NaHCO3溶液中加入等体积0.1mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1mol•L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验溶液中是否含有Fe2+时,所用KMnO4溶液用硫酸酸化 | |
| B. | 检验溶液中是否含有Br-时,所用AgNO3溶液用盐酸酸化 | |
| C. | 检验溶液中是否含有SO32-时,所用BaCl2溶液用硝酸酸化 | |
| D. | 检验溶液中是否含有SO42-时,所用BaCl2溶液用硝酸酸化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 提取食盐后的母液$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{稀HCl}{→}$MgCl2溶液$\stackrel{电解}{→}$Mg | |
| B. | Cu$\stackrel{H_{2}O_{2},稀H_{2}SO_{4}}{→}$CuSO4溶液$\stackrel{蒸发,结晶}{→}$CuSO4•5H2O | |
| C. | 饱和食盐水$\stackrel{NH_{3}}{→}$$\stackrel{CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| D. | N2$→_{催化剂}^{H_{2}}$NH3$→_{催化剂}^{O_{2}}$NO→NO2$\stackrel{H_{2}O}{→}$HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 白色沉淀是CuI2,棕色溶液含有I2 | |
| B. | 滴加KI溶液时,转移1mol电子时生成0.5mol白色沉淀 | |
| C. | 通入SO2时,SO2与I2反应,I2作还原剂 | |
| D. | 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com