
| A、1molCH3+(碳正离子)含有9 NA个电子 |
| B、2.5molHe 中含有10 NA个质子 |
| C、6.02×1022 个H2SO4分子在溶液中可电离出2NA个H+ |
| D、1molFe与盐酸完全反应可失去电子的物质的量为2NA |


科目:高中化学 来源: 题型:
| A、酸性:HClO4>H3PO4>H2SO4 |
| B、碱性:KOH>NaOH>Mg(OH)2 |
| C、离子半径:O2->F->Cl->Na+ |
| D、氢化物稳定性:H2S>HF>H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热至50℃,溶液的Ca2+的浓度增大 | ||
B、该温度下Ca(OH)2的溶解度为
| ||
| C、该饱和石灰水中,水电离出的OH-的浓度为10-12mol/L | ||
D、加入生石灰并恢复至常温后,
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2F2+2H2O=4HF+O2↑ |
| B、2Na+2H2O=2NaOH+H2↑ |
| C、CaO+H2O=Ca(OH)2 |
| D、Cl2+H2O=Hcl+HclO |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、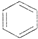 +HNO3 +HNO3
 +H2O +H2O | |||
B、CH2=CH2+Br2→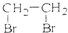 | |||
C、CH3CH2OH+CH3COOH
| |||
D、CH4+Cl2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L氦气所含核外电子数为4NA |
| B、16g CH4与18g NH4+所含质子数相等 |
| C、在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移2NA个电子 |
| D、常温常压下,23g NO2和N2O4混合气体中含有的原子数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、通常情况下,烷烃跟强酸、强碱、强氧化剂不起反应 |
| B、互为同系物的烷烃分子,它们的相对分子质量相差的一定是14的倍数 |
| C、甲烷跟氯气的反应属于取代反应 |
| D、烷烃在空气中燃烧只能生成CO2和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
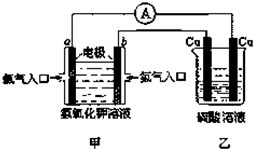 根据如图所示的装置(甲中电极均为惰性电极)判断下列叙述中正确的是( )
根据如图所示的装置(甲中电极均为惰性电极)判断下列叙述中正确的是( )| A、利用该反应可持续生产硫酸铜,直至硫酸耗尽 |
| B、甲中b电极的电极反应为:4OH--4e-=2H2O+O2↑ |
| C、通电初期乙中的总反应为:通电Cu+H2SO4═CuSO4+H2↑ |
| D、反应过程中甲、乙装置的pH都逐渐减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com