
| A. | 18.9 g HNO3 | B. | 3.612×1024个HCl分子 | ||
| C. | 0.2 mol H3PO4 | D. | 0.2 NA个CH4分子 |
分析 0.3mol H2O含有氢原子物质的量为0.3mol×2=0.6mol,由N=nNA可知,H原子个数相同,则H原子的物质的量相等.
A.根据n=$\frac{m}{M}$计算硝酸物质的量,由于每个硝酸分子含有1个H原子,故含有H原子物质的量等于硝酸物质的量;
B.根据n=$\frac{N}{{N}_{A}}$计算HCl物质的量,由于每个HCl分子含有1个H原子,故含有H原子物质的量等于HCl物质的量;
C.由于每个H3PO4分子含有3个H原子,故含有H原子物质的量是H3PO4物质的量3倍;
D.根据n=$\frac{N}{{N}_{A}}$计算CH4物质的量,由于每个CH4分子含有4个H原子,故含有H原子物质的量是CH4物质的量的4倍.
解答 解:0.3mol H2O含有氢原子物质的量为0.3mol×2=0.6mol,
A.18.9 g HNO3物质的量为$\frac{18.9g}{63g/mol}$=0.3mol,由于每个硝酸分子含有1个H原子,故含有H原子物质的量为0.3mol×1=0.3mol,故A不符合;
B.HCl物质的量为$\frac{3.612×1{0}^{24}}{6.02×1{0}^{23}mo{l}^{-1}}$=6mol,由于每个HCl分子含有1个H原子,故含有H原子物质的量为6mol×1=6mol,故B不符合;
C.由于每个H3PO4分子含有3个H原子,故含有H原子物质的量为0.2mol×3=0.6mol,故C符合;
D.CH4物质的量为$\frac{0.2{N}_{A}}{{N}_{A}mo{l}^{-1}}$=0.2mol,由于每个CH4分子含有4个H原子,故含有H原子物质的量是0.2mol×4=0.8mol,故D不符合,
故选C.
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的有关计算.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 两种不同元素的原子和离子 | B. | 同一元素的两种离子 | ||
| C. | 同一元素的原子和离子 | D. | 两种不同元素的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
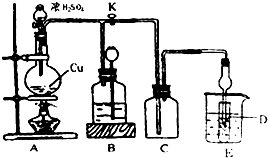
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 减小 | B. | 增大 | C. | 维持不变 | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn为正极 | B. | 负极反应式:O2+4H++4e-→2H2O | ||
| C. | 正极发生氧化反应 | D. | 电解液肯定不是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 客观事实 | 理论解释 |
| A | Na+比Na原子稳定 | Na+最外电子层有8个电子而Na只有1个 |
| B | 熔化状态下NaCl能导电而NaCl晶体不能导电 | 熔化状态下的NaCl中存在离子而NaCl晶体中没有离子 |
| C | 钾原子比钠原子更易失去电子 | 钾的核电荷数比钠的多 |
| D | 纯碱溶液能使湿润的紫色石蕊试纸变蓝色 | 纯碱能电离出OH-而使石蕊试纸变蓝色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴入KSCN溶液显红色的溶液中:K+、Fe2+、SO42-、Cl- | |
| B. | 1 mol•L-1的烧碱溶液中:S2-、SO32-、SO42-、K+ | |
| C. | 使淀粉碘化钾试纸变蓝的溶液:Cs+、Ba2+、S2-、Cl- | |
| D. | 含有大量HCO3-的澄清透明溶液中:K+、NH4+、SO42-、MnO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1gH2所含的原子个数 | |
| B. | 4g氮气所含的原子个数 | |
| C. | 16gO2所含的分子个数 | |
| D. | 23g金属Na全部转变为金属离子时失去的电子个数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com