
| ʵ����� | m��Mg��/g | �������/mL | Һ����ƿ��Һ�����/mL | ����������/mL | �������/mL | ����1mol�����/L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | X | |
| 2 | 0.115 | 10.0 | 121.0 | 8.0 |
| ʵ����� | m��Mg�� g |
�������mL | Һ����ƿ��Һ�����mL | ����������mL | Bƿ��һ��Һ�����mL | ˮ������ٷֺ��� | ����1mol�����L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | VB | a% |
| 0.1065L��24.3g/mol |
| 0.100g |
| 0.119L��24.3g/mol |
| 0.115g |
| 25.9+25.1 |
| 2 |
| 25.5-24.5 |
| 24.5 |
| (106.5-VB)��10-3L��(1-a%)��24.3g/mol |
| 0.1g |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| �� |
| ||
| �� |
| 2016��6 |
| 2688��5 |
| 2016��6 |
| 2688��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ���� |
| ʵ�鲽�� | ���� | ��������� |
| ��һ�� | ȡ����Һ��װ���Թܣ����� ���е��뼸��KSCN��Һ�� |
|
| �ڶ��� | ����Һ��ɫ��ȥ����˵������Fe2+�� �������Ա仯����˵������Fe2+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ʵ�鲽�� | ���� | ��������� |
| ��һ�� | ȡ����Һ��װ���Թܣ����Թ��е��뼸��KSCN��Һ�� | |
| �ڶ��� | ����Һ��ɫ��ȥ����˵������Fe2+�� �������Ա仯����˵������Fe2+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ���Ϻ���������������ѧ����ĩ��ѧ������⻯ѧ�Ծ��������棩 ���ͣ�ʵ����
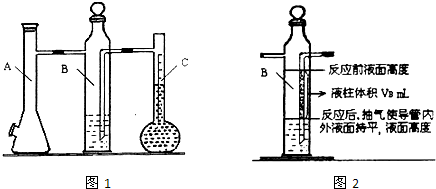
��ͼ1��ʾ��ʵ��������ȡ�����һ�ּ���װ�á�

��1��������������������Եķ���_______________________��
��2��������ͼ1��ʾװ�ÿ�����ȡ���Ӧ��״����������Ӧ�Ƿ���Ҫ��������________________________���塣
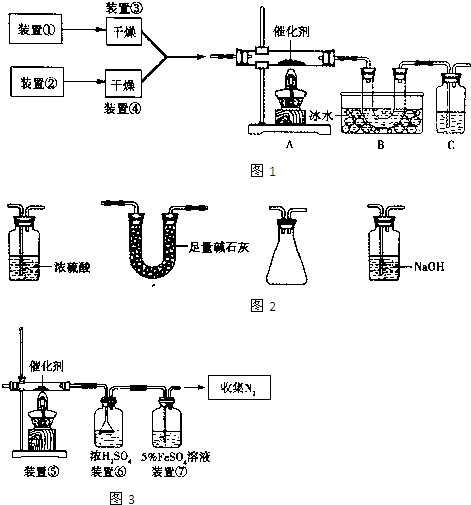
ijͬѧ�����ͼ2��ʾװ�ã��ô�������16.9%ϡ���ᷴӦ��ȡNO���岢̽�����������ļ�̬����ش��й����⡣

��3����֪16.9%ϡ������ܶ�Ϊ1.10g/cm3���������ʵ���Ũ��Ϊ____________��������������λС������������63%����������16.9%ϡ����500mL������IJ��������в��������ձ��� ��
��4������ֹˮ��a���ر�ֹˮ��bʱ��Aװ�õĸ�����й۲쵽��������_______________________��Bװ���ձ���Һ���������__________________________________����Aװ�������弸����ɫʱ����ֹˮ��b���ر�ֹˮ��a������Cװ���ռ�NO���塣
��5����֪���з�Ӧ���Է�����Fe2O3+3KNO3+4KOH 2K2FeO4+3KNO2+2H2O����Aװ���е�ϡ���ἴʹ����Ũ���ᣬҲ��������+6�۵����Ļ������ԭ����________��
2K2FeO4+3KNO2+2H2O����Aװ���е�ϡ���ἴʹ����Ũ���ᣬҲ��������+6�۵����Ļ������ԭ����________��
a��HNO3 �������Ա�KNO3��
b����Ӧ���¶Ȳ���
c��HNO3 �����ȶ��Ա�KNO3��
d��FeO42�����ܴ�����������Һ��
��6������������ҩƷ���Թܺͽ�ͷ�ιܣ�0.1mol/LKSCN��Һ��0.2mol/L����KMnO4��Һ��0.1mol/LKI��Һ����ˮ�ȡ��������һ����ʵ�飬̽��Aװ���ձ�����ȫ��Ӧ�������ܵļ�̬����д����ʵ�鱨�棺
|
ʵ�鲽�� |
���� |
��������� |
|
��һ�� |
ȡ����Һ��װ���Թܣ����� ���е��뼸��KSCN��Һ�� |
|
|
�ڶ��� |
|
����Һ��ɫ��ȥ����˵������Fe2+�� �������Ա仯����˵������Fe2+�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com